多价、多特异性和修饰的纳米抗体在疾病治疗中的研究进展及应用
近日,Frontiers in immunology期刊发表了题为“Research Progress and Applications of Multivalent, Multispecific and Modified Nanobodies for Disease Treatment”的论文。该论文由天津大学、天津医科大学总医院和斯洛文尼亚新戈里察大学联合发表。新戈里察大学Ario de Marco教授和天津大学的黄鹤教授为论文通讯作者,博士生王杰文和助理研究员康广博博士为论文第一作者。论文下载地址:https://doi.org/10.3389/fimmu.2021.838082
要点速览
纳米抗体正逐步被视为一种传统单克隆抗体的替代品,并被用于临床治疗等应用。它们不仅是备选方案,而且其独特的功能特性使生物疗法的应用得以扩大,并改变了疾病治疗的模式。纳米抗体具有体积小和易于设计的双重优势。图一所示,结合纳米抗体的优势特性设计特定应用下的多价/多特异性纳米抗体结构得到了进一步发展。
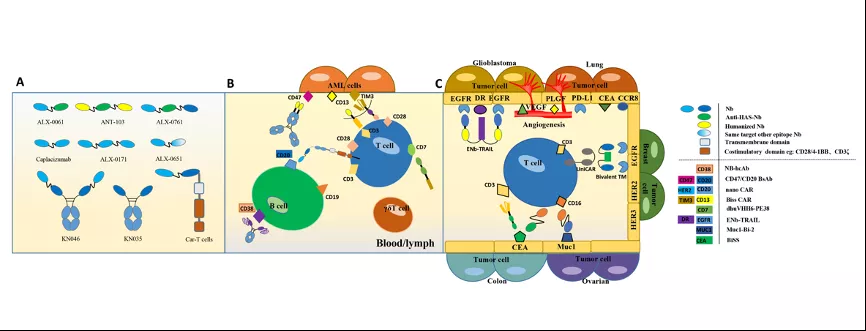
图一. 多价/多特异性纳米抗体的结构和作用机制▲
近年来,无论是几何构型的可能性,还是功能化策略都已被广泛地探索,以提供相对于单个纳米抗体具有更好效果的功能大分子。多价/多特异性纳米抗体被开发用于成像和多种癌症治疗,并在动物模型中显示出显著的效果。多特异性纳米抗体具有同时阻断更多独立信号通路的能力,这是其在避免肿瘤耐药性方面的关键优势。此外,它们的质量明显小于单克隆抗体,在实体肿瘤中具有更好的组织穿透性。当纳米抗体作为细胞外抗原识别结构域应用于CAR-T细胞治疗时,一定程度能够解决单链抗体寡聚化导致的强直信号传导、T 细胞衰竭和体内表现不佳等缺点,并且可以通过靶向多个表位有效提高特异性,从而减少副作用。这在治疗恶性淋巴瘤、急性髓细胞白血病、急性淋巴母细胞白血病、多发性骨髓瘤和实体瘤方面具有很大的潜力。除了癌症治疗,基于纳米抗体构建的成像试剂和多特异性抗体药物在检测和治疗神经退行性疾病、自身免疫疾病、代谢疾病、传染病以及作为毒素解毒剂方面的价值都得到了证明。值得一提的是,基于多特异性纳米抗体结构开发的SARS-CoV-2中和抗体已经进入临床,以克服病毒突变引起的耐药性,从而削弱变体的生存。鉴于该领域的大量研究,可以预期未来将有越来越多的多聚纳米抗体分子进入到后期临床试验。
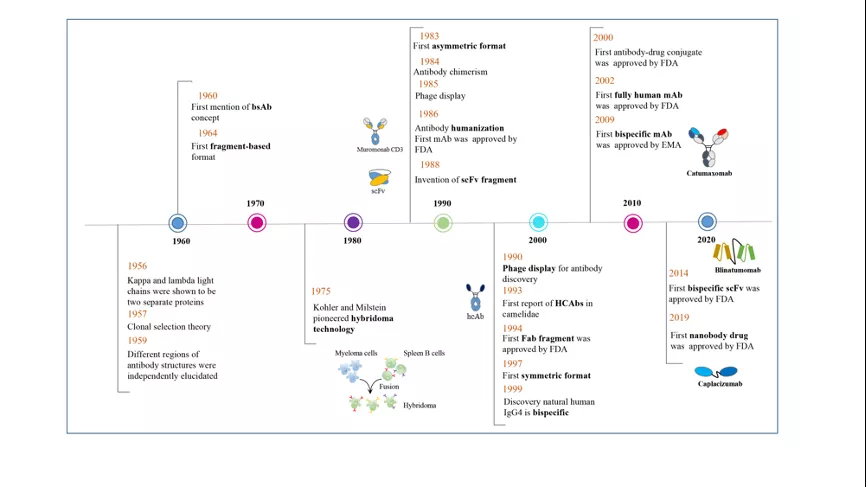
图二. 多价/多特异性纳米抗体概念发展和技术创新时间表▲
应用一、癌症治疗研究
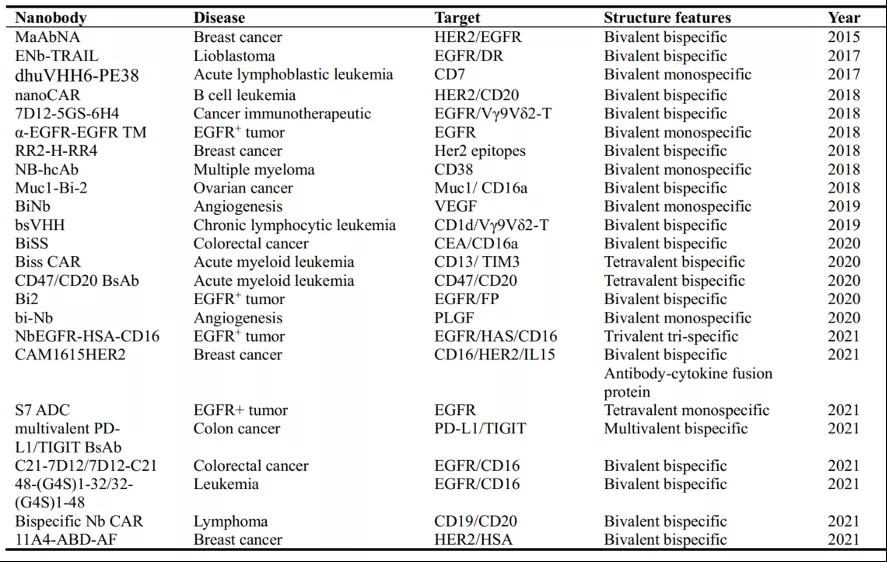
纳米抗体免疫试剂在α粒子辐射、光动力治疗以及体内成像领域取得了重大进展 [1]。如表一所示,尽管目前只有KN035 恩沃利单抗在去年11月被NMPA批准上市并用于治疗晚期结直肠癌,没有其他基于纳米抗体结构的药物被批准用于癌症治疗。但已经有大量的基于多价、多特异性纳米抗体及其修饰结构的生物制剂在多种癌症治疗中进入了临床研究 [2,3]。如表二所示,纳米抗体易于工程化改构的特性使得构建物具有广泛的生物分布和清除模式,在多种癌症模型中被应用。
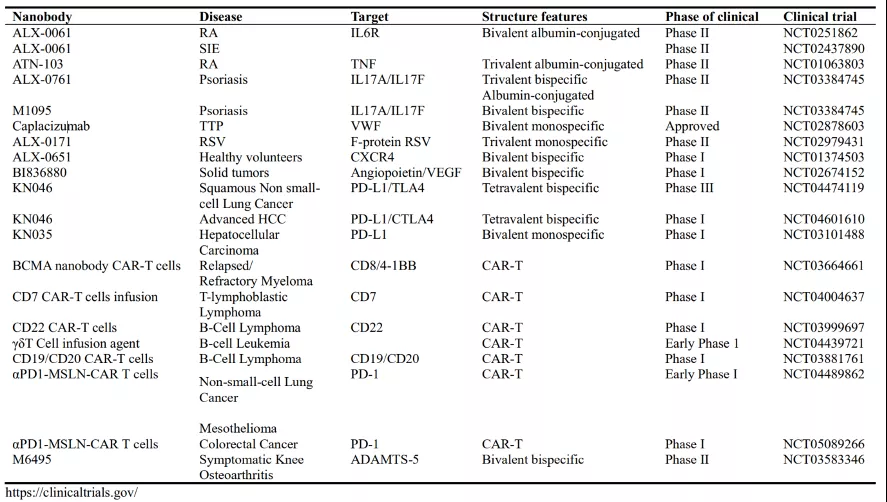
表一. 进入临床试验阶段的多价单/双特异性纳米抗体▲
应用二、自身免疫性疾病研究
抗体是治疗免疫疾病的一种有力手段。目前,已获批用于治疗类风湿性关节炎、炎症性肠病、1型糖尿病、牛皮癣、红斑狼疮和多发性硬化症等自身免疫性疾病[4]。包括纳米抗体在内的小型化抗体是目前许多用于治疗免疫疾病的优化型抗体方案,对一些治疗性抗体缩短其半衰期从而减少存留时间可能有利,提高了抗体安全性。如表三所示,免疫性疾病发病机制涉及多种炎性因子的过表达,因此同时封闭多个炎性细胞因子能够防止免疫逃逸从而取得更好的治疗效果。
应用三、感染性疾病研究
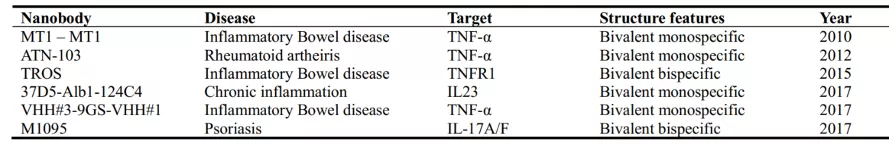
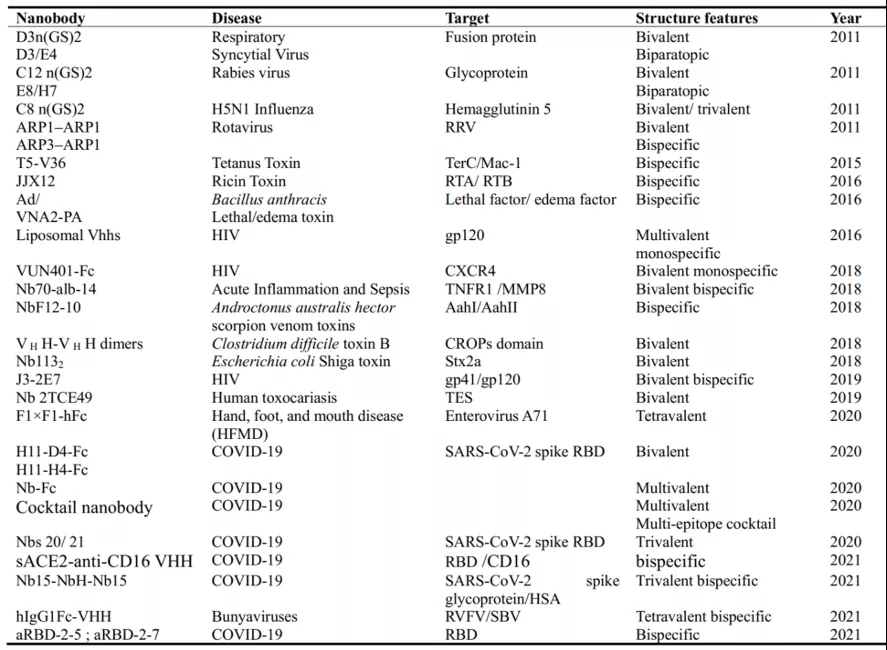
开发针对多重耐药细菌有效的新疫苗和抗生素是困难和耗时的。如表四所示,近年来,具有中和毒素活性的纳米抗体已被研究用于治疗感染病,如艰难梭菌、炭疽芽孢杆菌、蓖麻毒素和炭疽导致的毒素感染。此外,纳米抗体代表了对抗病毒爆发的另一种抗感染治疗选择[5,6]。
其他应用
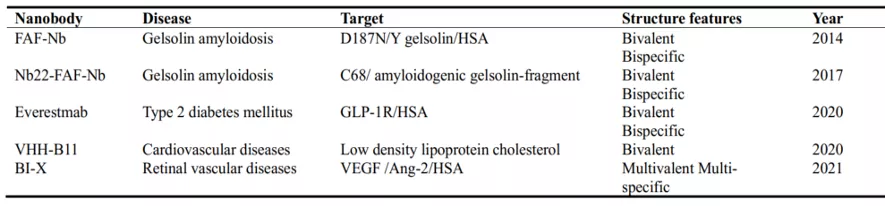
尽管基于纳米抗体的生物制剂大部分应用癌症自身免疫疾病和感染病的研究领域,基于其独特的工程化优势,它们的潜在用途也在二型糖尿病、眼科疾病和神经系统疾病等其他领域得到了证实,如表五所示。
结语
该论文报道了用于疾病治疗的工程化纳米抗体的研究趋势,因为这方面还没有系统地总结。作者分析了近年来在癌症、免疫疾病和抗感染治疗中使用多特异性纳米抗体和其他多聚纳米抗体形式的研究,以探讨这类大分子的功能特性。总之,过往的研究成果表明,基于纳米抗体构建的多聚体和功能化分子将成为未来诊断和治疗试剂的重要组成部分。
参考资料:
[1] Yang EY, Shah K. Nanobodies: Next Generation of Cancer Diagnostics and Therapeutics. Front Oncol (2020) 10. doi: 10.3389/fonc.2020.01182
[2] Tolmachev V, Orlova A, Sorensen J. The emerging role of radionuclide molecular imaging of HER2 expression in breast cancer. Semin Cancer Biol (2021) S1044-579X (20) 30210-8. doi: 10.1016/j.semcancer.2020.10.005
[3] Kang G, Hu M, Ren H, Wang J, Cheng X, Li R, et al. VHH212 nanobody targeting the hypoxia-inducible factor 1alpha suppresses angiogenesis and potentiates gemcitabine therapy in pancreatic cancer in vivo. Cancer Biol Med (2021) j.issn.2095-3941.2020.0568. doi: 10.20892/j.issn.2095-3941.2020.0568
[4] Zian Z, Berry SPD-G, Bahmaie N, Ghotbi D, Kashif A, Madkaikar M, et al. The clinical efficacy of Rituximab administration in autoimmunity disorders, primary immunodeficiency diseases and malignancies. Int Immunopharmacol (2021) 95:107565-. doi: 10.1016/j.intimp.2021.107565
[5] Marston HD, Paules CI, Fauci AS. Monoclonal Antibodies for Emerging Infectious Diseases - Borrowing from History. N Engl J Med (2018) 378:1469-72. doi: 10.1056/NEJMp1802256
[6] Levi-Schaffer F, de Marco A. COVID-19 and the revival of passive immunization: Antibody therapy for inhibiting SARS-CoV-2 and preventing host cell infection: IUPHAR review: 31. Br J Pharmacol (2021). doi: 10.1111/bph.15359
- 上一篇: Nanobody vs ScFv
- 下一篇: 免疫疗法黑科技!纳米抗体+声控细菌可有效对抗肿瘤

