EMBO报道免疫疗法新突破:靶向ASC纳米抗体可有效减缓慢性炎症
近期,EMBO 杂志报道了一项抗体靶向疗法的新发现,来自波恩大学和圣保罗大学的研究人员成功合成了一种纳米抗体,这种纳米抗体能够溶解组织中激活免疫系统的分子复合物,从而有助于减缓导致关节炎或神经退行性疾病等的炎症反应。

DOI:https://doi.org/10.15252/emmm.202115415
类似高档住宅的报警电话,人体内的细胞也有一个复杂的警报系统,即炎性小体(inflammasome)。它的核心成分是ASC 蛋白(也被称为凋亡相关斑点样蛋白)。ASC斑点(ASC-speck)是由分子量大小为22 kDa的ASC蛋白聚集成大分子的二聚体,这种方式产生的ASC斑点会引发细胞间大量信使物质的积累,向免疫系统“求救”。同时细胞膜会被破坏,产生的孔洞直接导致信使分子逃脱并发出警报,从而导致免疫系统产生炎症反应。
在最新这项研究中,来自波恩大学医院先天免疫研究所的Bernardo Franklin教授解释说:“这些孔洞最终会导致细胞凋亡,在某一时刻细胞会爆炸并将全部胞质释放到组织中,而此时信使物质突然被释放就像最后一次呼救一样,会触发免疫系统产生强烈的炎症反应,从而抑制感染。”这就是为什么先天免疫防御机制非常重要的原因。
然而在这个过程中,ASC 斑点也会在组织中积累,并且可能会持续很长时间。先前的小鼠实验证明,即使在威胁已经解除之后,ASC斑点的活动也会激活免疫系统,这就可能导致慢性炎症的产生并且严重损害到肌体组织。

不同颜色表示的ASC 斑点,是 ASC蛋白聚集形成的复合物(来源:Franklin Lab / University of Bonn)
为了研究和预防这种不良影响的发生,研究人员生成了特异性靶向ASC并可以溶解斑点的纳米抗体。通过给羊驼体内注射ASC 蛋白,可从羊驼的血液中获得 ASC 纳米抗体的DNA信息。然后利用噬菌体展示技术进行大量生产,研究人员得到了纳米抗体VHHASC,进一步的体内实验中他们发现,在小鼠急性痛风或慢性类风湿关节炎(RA)模型中,VHHmASC全身治疗有效地抑制了尿酸钠(MSU)晶体或mBSA关节内刺激引起的炎症。不仅如此,研究人员还发现,VHHASC只能通过炎症小体激活的细胞死亡后形成的膜孔访问胞质ASC斑点,因此,不影响对宿主防御重要的早期细胞因子(IL-1β)的产生。
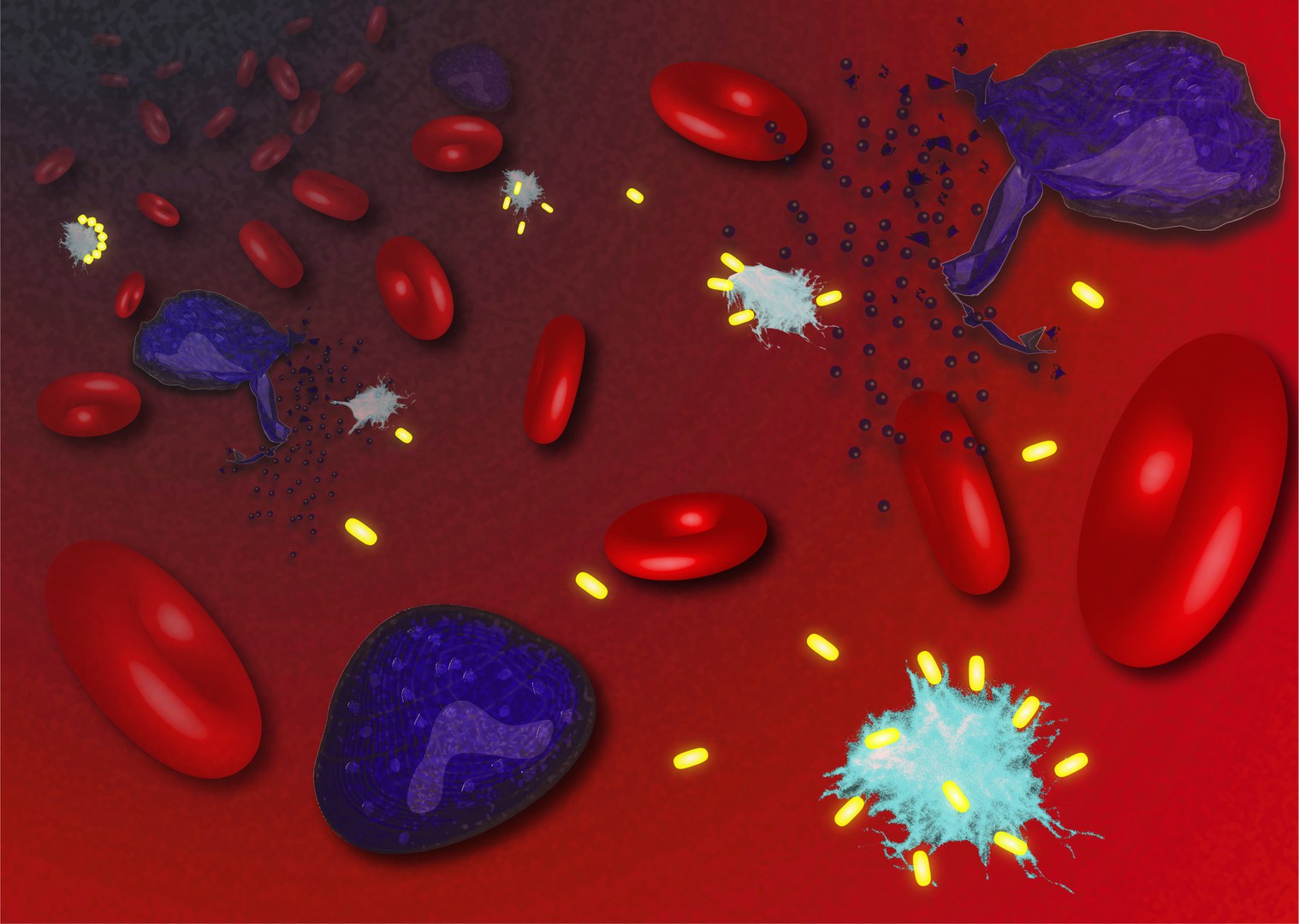
当受感染的细胞(紫色)破裂时会释放 ASC 斑点(浅蓝色)。纳米抗体VHHmASC(黄色)使斑点分解,炎症减少(来源:Franklin Lab / University of Bonn)
与正常抗体相比,纳米抗体尺寸非常小,穿透性比普通单克隆抗体更强,同时还能避免正常单克隆抗体会为免疫系统提供额外刺激,可能加剧炎症的特性,因此非常适合分解ASC类分子复合物。
作者指出,这项研究结果之所以有趣,除了因为VHHASC是第一个能够分解预制的炎性小体,同时保留其在宿主防御中的功能的生物制剂外,还有另一个原因——VHHASC或能减缓与神经退行性疾病相关的大脑损害。
之前研究表明,导致阿尔兹海默症的关键蛋白——β淀粉样蛋白(amyloid-β)的堆积伴随着先天性免疫系统的激活。当炎症反应发生时,小神经胶质细胞会促进炎症体依赖性的ASC斑点样蛋白释放,ASC会快速与β淀粉样蛋白结合,增加了β淀粉样蛋白低聚物和聚合物的形成。基于此项研究,该团队推测,纳米抗体也许有可能减缓这一过程。
据悉,未来Franklin教授团队将在后续研究中调查这种可能性,并继续推进VHHmASC的成药性研究。期待他们能为疾病治疗带来新方法。
参考资料:
1.Nanobodies dismantle post-pyroptotic ASC specks and counteract inflammation in vivo
2.Carmen Venegas, Sathish Kumar, Bernardo S. Franklin et al. Microglia-derived ASC specks cross-seed amyloid-β in Alzheimer’s disease. Nature, Published online: 20 December 2017, doi:10.1038/nature25158
3.New approach against chronic inflammation: Treating mice with so-called 'nanobodies'
- 上一篇: 免疫疗法黑科技!纳米抗体+声控细菌可有效对抗肿瘤
- 下一篇: 基于纳米抗体的CAR-T细胞疗法

