CAR-T和TCR-T细胞免疫治疗的前景与挑战
嵌合抗原受体(CAR)和T细胞受体(TCR)修饰的T细胞是当前过继性细胞治疗ACT技术中两大最新的技术,实现了从基础免疫学机制研究到临床免疫治疗应用的转变。因其能够表达人工合成受体并能特异性识别靶细胞,CAR-T和TCR-T正成为振奋人心的癌症治疗方法;对于慢性感染及自身免疫性疾病,它同样具有广泛的-应用前景。合成生物学原理,以及免疫学和基因工程的进步,使得制备特异性功能增强型的人T细胞成为可能。在CD19特异性CAR-T细胞应用于B细胞白血病及淋巴瘤的临床试验中,成人和儿童患者均显示出持续性缓解效果。近期制药工业界的加入,使得工程化T细胞的应用前景发生了巨大的变化。在此综述中,爱康得生物将和大家一起分享国外临床科研工作者对肿瘤过继免疫治疗中已面临的挑战和未来机遇的探讨。
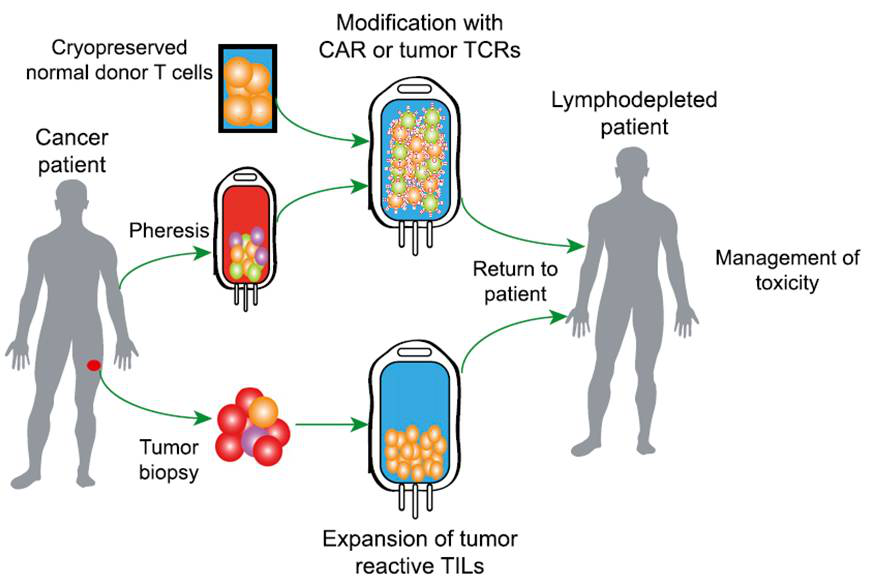
目前有三种使用效应T细胞的过继细胞疗法正朝着注册审批的方向行进(图1)。肿瘤浸润性淋巴细胞(TILs)虽发展缓慢,但数十年来一直进步,近期一项针对转移性黑色素瘤的国际III期随机试验已经开始。新近组建的Lion Biotechnologies公司正商业化应用TILs治疗黑色素瘤和其他有T细胞浸润的肿瘤。
与TILs相比,开发转基因的方法克服对肿瘤特异性T细胞免疫耐受。这种方法通过转导嵌合抗原受体(融合抗原结合域及T细胞信号结构域)或者TCRα/β异二聚体,使T细胞能够重新高效的识别靶细胞。通过输注能够识别特异靶标的基因修饰T细胞,赋予免疫系统以新的非自然免疫活性。这种方法除了能像细胞毒性化疗和靶向治疗快速杀灭肿瘤外,还避免了疫苗和T细胞检查点疗法的延迟效应。
除了极个别情况外,细胞疗法的个性化指的是自体的、源于患者的T细胞。正因如此,过继细胞治疗的开发主要依赖于学术界与制药行业的紧密合作。在这个模式中,学术界与工业界共存,前者开发和检验细胞工程技术的新思路,后者扩大和实现新方法在医疗健康领域中的影响力。这种学界和工业界的合作伙伴关系已经在全球的许多机构中出现,包括宾夕法尼亚大学与诺华,贝勒医学院与BluebirdBio、Celgene公司,纪念斯隆-凯特林癌症中心、哈钦森弗莱德癌症研究中心与JunoTherapeutics公司,国立癌症研究所与Kite Pharma,西比曼与中国解放军总医院。总体来说,现在有数十家细胞治疗领域的企业总投资达数十亿美元。
这种合作关系的影响力仍不明确,学术界的学术自由与大型企业专注于价值相遇必将产生冲突,寻求校外的项目资金支持和知识产权的归属问题,将成为创造这个领域的学者与谋求获得技术授权的制药公司之间激烈争论的话题。
从历史角度来看,早在二十几年前,就已应用基因修饰T细胞对晚期艾滋病患者进行过继细胞治疗,早期来源于HIV患者的临床试验结果提供了目前应用于肿瘤过继细胞治疗的理念,例如CAR-T细胞可以在HIV-1/AIDS患者体内存活十余年。最初这些试验是为了控制HIV-1感染的耐药性,然而,目前该领域的挑战是开发细胞治疗的潜力,用来清除寄宿的耐受抗病毒治疗的HIV-1。GeroHutter等人进行的一项特别的试验使得该领域充满活力,感染HIV-1的患者,在接受同种异体造血干细胞(HIV阴性CCR5Delta32纯合子)移植的过继细胞治疗后被治愈。有许多方法诱导细胞产生对HIV-1感染的内在抗性,以及通过基因修饰的过继细胞输注疗法来靶向寄宿的HIV-1。最近研究表明,使用特异性CD8+CTLs进行过继细胞治疗可以清除人源化小鼠体内潜在的HIV-1病毒,为利用基因修饰的T细胞治疗HIV-1感染和其他内源性免疫系统不能控制的慢性感染提供了理论基础。随着构建具备人体免疫系统小鼠技术的不断提高,使用ACT治疗HIV-1感染的进程将得到非常大的推进。
|
图1:目前细胞治疗的几种途径。通过修饰,使正常供体细胞的同种异体排异反应失活,同时使用抗肿瘤的CAR或TCR武装它;或利用抗肿瘤分子武装患者自体细胞。在实体肿瘤中,活检标本可用来分离TILs并进行扩增。大多数情况下,病人在接受抗肿瘤淋巴细胞输注前需要接受必要的预处理,并须谨慎处置治疗引发的毒性。
利用调节性T细胞(Treg)抑制有害的免疫应答正引发越来越大的兴趣。这一方法的有效性已经在自身免疫性疾病和同种异体移植排斥反应的临床前模型中得到验证。在小鼠体内过继回输调节性T细胞能防止致命性移植物抗宿主病和自身免疫性糖尿病。经历同种异体造血干细胞移植的患者,接受扩增的脐带血Treg细胞已被证明是安全和可行的。研究人员开发了许多不同的细胞培养方法,以提高自然的和诱导的Treg细胞的扩增和功能。爱康得生物编译作者认为对不同细胞培养方案的需求差异,可能是由于Treg细胞和效应T细胞在信号转导方面的差异所致。合成生物学及生物工程原理已被用于Treg细胞,例如,CAR-Treg在自身免疫疾病的临床前研究模型中崭露头角,将CAR应用于Treg细胞的概念集中于通过CAR使Treg细胞聚集于易受攻击的组织,用来抑制那里的自身免疫。利用CAR修饰小鼠Treg细胞靶向髓鞘碱性蛋白特异性T细胞,可以防止自身免疫性脑炎。基于此理念,分别寻找结肠和胰岛的靶向抗原可防止结肠炎和糖尿病。
动物模型在细胞治疗开发中起着关键的作用。目前研究者主要使用两种模型:一是同基因型小鼠模型,使用小鼠T细胞和小鼠抗原;二是异种移植瘤模型,使用免疫缺陷型小鼠和人源T细胞及人源肿瘤细胞。在细胞治疗发展的几十年里,使用这些模型经常会得出矛盾和相冲突的结论。细胞治疗中大量的可变因素是产生这些冲突的原因之一。CAR的结构、T细胞的类型构成(CD4/CD8,或2者兼有)、共刺激分子的选择、基因转导的方法、细胞体外扩增的时间和方法、宿主是否清髓、肿瘤类型和肿瘤负荷量等都必须准确掌控,才能获得准确的结论。比如,在异种移植瘤模型中已发现,体外扩增中不使用CD28刺激有益于使用CD28作为共刺激信号的CAR。
同基因型小鼠模型具有完整免疫系统的优点,而异种移植模型具有能够研究人类细胞的优点。一些嵌合抗原受体的研究使用异种移植模型准确预测其有效性。这些系统未能成功预测到任何毒性,特别是接受抗CD19CAR-T细胞治疗的小儿急性淋巴细胞白血病(ALL)产生的细胞因子释放综合征(CRS)(见下文)。尽管同基因型小鼠模型能预测疗效,但是尚未能模拟CRS,一部分是由于鼠源和人源T细胞在体外激活和扩增能力存在细微而重要的差别。作为临床试验显然专注于人源T细胞,研究人源T细胞共刺激信号的影响变得至关重要,且为使用异种移植瘤模型提供支持。更复杂的模型是使用人源化小鼠如MISTRG strain(转基因表达人细胞因子如的CSF, M-CSF,IL-3, 和促血小板生成素的免疫缺陷型小鼠)为人源细胞提供物种特异性细胞因子的支持,以便改善植入的这些细胞,并可能同时构造人源细胞有效性和毒性模型。其他混合型模型,如在SCID/beige小鼠中使用人T细胞与小鼠单核细胞系相互作用,可能会提供更深入的理解。但是,与人源化的小鼠模型相比,从真正奏效的同基因型小鼠模型得到的数据更不易让人迷惑。但目前异种移植模型所产生的数据的可操作性仍需提升。因此,同基因模型和人源化异种移植模型提供的信息可以互补,同源系统非常适合在完整的免疫细胞环境下研究鼠细胞生物学,而人源化系统可允许人体细胞的植入和人细胞与细胞之间在体内的相互作用。
过去的20年中CAR的设计已经取得了长足的进展(图2)。1991年有3个实验室报道了第一代CAR的设计。Kuwana等人最先构造了嵌合受体,使T细胞不依赖于MHC-I类分子识别靶细胞。Roberts、Finney和 Lawson 率先构造了含有CD28或4-1BB共刺激分子的二代CAR。在临床前模型中,使用基于CD28的体外扩增体系,在异种移植瘤模型中 4-1BB比CD28对CAR的功效更有益。两种CAR模型都显示出临床前和临床疗效。Long等人的最近研究表明,基于CD28构造的CAR加强并加速T细胞衰竭,而基于4-1BB构造的CAR减缓了T细胞衰竭。我们的研究结果与其结论一致,并且发现CD28内切域能传递使效应T细胞终末分化的信号。从这些研究中得出的周密的结论并不是说某个人源内切域必然比另一个好,而是说CD28信号是生产有效的临床T细胞制品的关键,而4-1BB提升了CAR-T细胞的持久性。
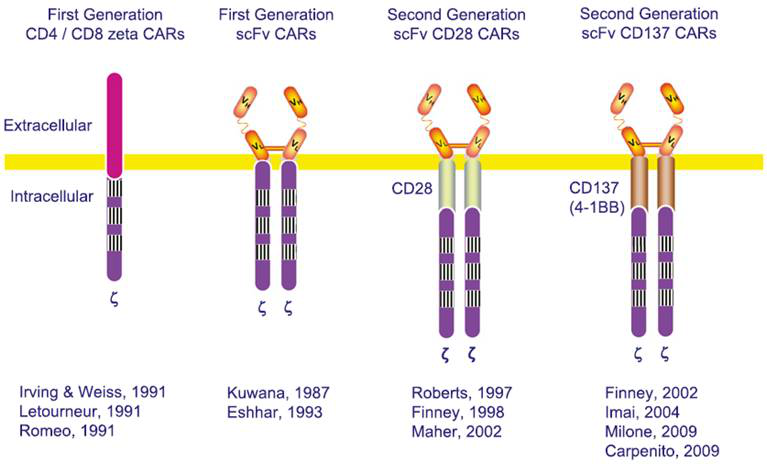
图2:CAR-T细胞的设计。第一代CAR引入了CD3ζ链或类似的信号域。基于抗体再定向的T细胞首先由Kuwana设计并由Eshhar完善。Roberts和Finney首先设计了整合CD28或CD137信号域的第二代CARs。
十多年来,许多ACT临床试验表明各类工程化的细胞产品相当安全,但有效性相对缺乏。过去的4年里,ACT的疗效发生了一场革命性变化,体现在工程化的T细胞可以在体内大量扩增,甚至在某些情况下可以持续性存活。这彻底的改变了ACT的疗效,尤其体现在CAR-T细胞应用于癌症治疗,但是在显示出疗效的同时,伴随有毒性。
CAR-T治疗骨髓源肿瘤最显著的毒性是CRS。高度增殖的T细胞能引起CRS,表现为高热和肌痛,不稳定的低血压和呼吸衰竭。这是一个意想不到的结果,因为在临床前动物模型中没有出现类似症状。从CRS观察中发现一个关键的点,除了预期的效应细胞因子INF-γ外,IL-6在CART治疗的细胞指数级增殖期间也会迅速提升。CRS可能直接与另一个毒性相关联,即巨噬细胞活化综合征。幸运的是,针对这些严重的CRS,寻找到了一种治疗方法,应用IL-6受体拮抗剂tocilizumab来阻断IL-6的作用。采用高度增殖的CART治疗ALL患者,确认了IL-6的出现和tocilizumab对严重CRS的疗效,并且我们观察到了双特异性T细胞衔接抗体blinatumomab引起的严重CRS具有类似机制。另一个重要发现是,严重的CRS几乎发生在高疾病负荷病人身上。这意味着将CAR应用于疾病早期患者身上,在疾病恶化之前使用CART来杀灭肿瘤,发生严重CRS风险将大大降低。
T细胞增殖可直接导致CRS。它不依赖于改造的T细胞的抗原特异性,即使CAR是相同的,治疗不同的疾病有可能CRS风险和症状也会有所不同。例如在治疗CLL和弥漫大B时CRS较轻而治疗ALL时CRS相对较重。除了CRS,还存在由工程改造的T细胞的抗原特异性导致的“靶向”毒性。例如溶瘤综合征,它直接是由肿瘤细胞的裂解而导致的。当CARs靶向于B细胞表面表达的靶点如CD19时,会引起B细胞发育不良,这就是一个“靶向”毒性,但却错误的攻击了正常组织细胞的结果。只要CD19CAR-T细胞长时间存在,B细胞发育不良的情况就不会改善,因此,B细胞缺乏可作为CAR-T疗效持续的标志。B细胞发育不良与CD20特异性单抗治疗一样会造成严重的低丙种球蛋白血症,需要静脉注射免疫球蛋白。不像CD20单抗rituximab引起的相对较轻的低丙种球蛋白血症,CAR引起的长期B细胞发育不良,静脉注射免疫球蛋白非常必要。最近报告了输注改造的T细胞引发致命毒性的2个案例,有一例患者接受了HER2-CAR治疗,两例患者接受了靶向MAGE-A3的TCR-T细胞治疗。在这2个案例中,均是因为正常组织表达这些靶点,导致急性不可逆的心肺毒性。所有的靶向毒性均是由于改造的T细胞无法区别表达靶向抗原的正常细胞和肿瘤细胞所致。高亲和力TCR改造的T细胞引起的毒性可能与亲和力成熟过程有关,因为“非肿瘤靶向”的高亲和力TCR的产生在生理条件下将受到限制。在设计TCR的过程中,小心筛选高亲和力的TCRs,并研究其对靶蛋白之外的其他抗原表位的识别显得十分必要。根据已有报道,输注HLA-A2/MAGE-A3特异性的TCR-T细胞能够产生神经毒性。
CAR-T治疗白血病会引起神经系统症状,这是一个预期之外且目前尚不清楚的现象。几个研究小组报道,这些症状具有多样性但可自行消退,如谵妄、语言障碍、运动障碍、缄默症和癫痫发作。虽然与全身CRS的发生有些时间上的关联,当然也与CAR-T存在于脑脊液中相关,但是使用tocilizumab这些症状不会有改变。这些症状的机制与靶组织仍有待确认。
输注活化的T细胞存在引起自身免疫性疾病的风险。靶向黑色素瘤的ACT治疗可诱发白癜风。输注活化的T细胞产生如皮疹、结肠炎、垂体炎等毒性的报道较少。CAR修饰的T细胞尚未出现这些问题。输注同种异体T细胞存在抗宿主移植病的潜在风险。这可能会引起曾接受同种异体造血干细胞移植的患者的担心。幸运的是,从受体采集已耐受供体来源的T细胞(而不是捐献者),抗移植物宿主病的风险会非常低。当然有一种方法是利用自杀系统来限制毒性,如经典的caspase-9诱导表达系统,或包含特定表面靶点如CD20。在含有caspase-9诱导系统下,一种水溶性活化剂可激活Caspase系统导致T细胞凋亡。包含CD20基因修饰的CAR-T细胞,可用单抗如rituximab来清除“违规”的细胞。
近期实验室研究正在解决在科学与工程方面遇到许多挑战。下面我们谈一谈当前面临的挑战。
早期的细胞治疗主要是输注高分化的CD8+T细胞。这些CTL细胞具有很强的细胞毒性,但是输注后没有足够的复制能力,除了个别情况外,注入患者体内的T细胞持久性较差。目前普遍同时输注CD4+与CD8+T细胞,很可能是因为CD4+T细胞提供生长因子和其他信号以维持输注的CTL的功能和活性。另外,在小鼠中的研究有时候会误导处理人源T细胞的方法。例如,由于受到端粒退化的影响,人源T细胞的复制能力有限,在小鼠模型中却没有这个特点,而人CD4+细胞比小鼠CD4+细胞具有更强的细胞毒性。现在的问题是是否需要利用流式细胞术或其他的方法分离细胞亚群并进行独立培养。CD4+和CD8+T细胞最佳细胞培养条件不同,这因为CD4+和CD8+ T细胞信号转导途径不一样。此外,细胞分离法可去除对效应T细胞疗法存在潜在危害的Treg细胞。况且,需要从输注的T细胞中去除肿瘤细胞,对白血病患者而言,这尤其具有挑战性。然而,在GMP生产中有些技术使细胞制备成本大大增加,如通过流式细胞术或磁珠分选细胞可使成本迅速增加10000美元甚至更多。
与上述问题相关,输注处于什么分化阶段的T细胞最佳?对小鼠和人类的研究结果表明,naive或中心记忆细胞是最好的。对只有少量naive T细胞的老年人而言,如何获取这类细胞是个挑战,且化疗或其他疾病通常会进一步放大难度。从我们采用CD19 特异性CAR-T治疗白血病患者的数据中表明,扩增能力是预测成功的最重要的生物学标志。一种方法是在全血淋巴细胞中分离中心记忆或naive T细胞。与此相反,一个更简便粗放的方法是使用大量T细胞在特定培养条件下维持naive或中心型记忆细胞的扩增。后一种方法基于特异性共刺激信号可以促使细胞定向分化的原理。如CD28的刺激可使CD4细胞保持中心记忆细胞状态,4-1BB可以促使CD8中心记忆细胞的增殖。相反ICOS共刺激分子可以促使和稳定Th17细胞的生长。利用T细胞的干细胞样特性是非常有希望的,Wnt信号通路的激活可以促进记忆干细胞的增殖。
是否存在统一的最佳细胞制品配方?抑或针对不同的肿瘤需要不同的配方?
CD19 CAR-T治疗B细胞恶性肿瘤显示出的惊人且意想不到的疗效能否出现在治疗实体瘤患者身上还未可知。我们发现CAR-T在体外杀灭低分化腺癌细胞的效率类似于白血病。然而,仍然有待进一步确定是否需要修改细胞组成类型或细胞培养条件,用来优化实体瘤患者体内改造的T细胞的转运和持久性。与恶性血液疾病的散在分布不同,采用细胞工程的方法优化T细胞向实体瘤块转运,如成胶质细胞瘤和胰腺癌,可能会有所不同。已提出一种方法是利用靶向策略,如采用基因工程的手段,使用各种趋化因子或趋化因子受体促使T细胞向肿瘤部位富集。其他方法包括对肿瘤或患者进行预处理,如进行放疗,注射溶瘤载体以及在瘤内直接注射T细胞。
以往研究表明不同亚群的T细胞培养条件是不同的。这就提出一个问题,不同淋巴细胞亚群的T细胞是否需要不同的信号分子进行武装呢?为着手解决这个问题我们对CD4+和CD8+T细胞胞内区CD28,4-1BB和ICOS进行了评估。在异种移植腺癌的人源化小鼠中,我们发现采用ICOS信号域的CD4+CAR-T细胞更为优越,而CD8+T细胞常优选4-1BB。如此增加细胞制备的复杂度是否能使临床实验受益尚有待进一步确定。此外,最佳的T细胞亚群比例和信号分子的构造在不同的肿瘤微环境中很可能会有差异。比如在一些临床前肿瘤模型中改造的Th17细胞比Th1细胞更优越。
使用改造的T细胞最大的不确定性是利用生物合成技术诱导的新的、增强的细胞效应是否会引发意外的脱靶毒性。CAR-T细胞的非肿瘤靶向毒性和TCR细胞的脱靶毒性被格外关注。有多种方法可以缓解这些问题。我们发现利用编码CAR的mRNA转染T细胞,限制CAR仅在转染T细胞中表达,对评估出现的直接毒性有帮助。当出现毒性反应,停止细胞输注,毒性会迅速减弱。研究人员也提出了许多诱导基因修饰T细胞凋亡的方法。这些方法很可能都会被整合,以便按需清除T细胞,满足严格的安全需求。
基于正在进行的试验,表达CARS和TCRS的T细胞已经为广泛的商业应用准备就绪。华尔街的资源正推动这个曾因投资不足而被限制的领域的进步。在输注的T细胞中引入或删除基因,提供了能克服肿瘤免疫抑制微环境的新细胞制品,并且最后可能不需要使用免疫检查点封闭抗体。ACT先进的基因工程技术的到来,将会使利用合成生物学原理进行癌症、慢性感染和自身免疫性疾病的治疗取得显著进展。
- 上一篇: 这边的T细胞你清醒下,那边的肿瘤细胞你别装了
- 下一篇: CAR-T细胞免疫治疗技术与肿瘤精准免疫治疗