PD1/PDL1报告基因细胞株
1.产品背景
PD-1,也被称为程序性细胞死亡蛋白1或CD279(分化簇279),是一种细胞表面受体,为免疫球蛋白超家族成员,在T细胞和B细胞上表达。PD-L1作为PD-1最重要的配体,几乎在所有的肿瘤细胞系中都有表达。PD-1作为一种免疫检查点,参与多种肿瘤的进展。PD1与PD-L1结合后可抑制CD4阳性T细胞和CD8阳性T细胞的增殖和活化,同时介导白介素(IL)-2和干扰素(IFN)-γ分泌的下调,最终抑制T细胞免疫功能,形成免疫抑制肿瘤微环境,使肿瘤细胞获得免疫逃逸。
通过阻断PD1/PD-L1信号传导通路可逆转免疫抑制肿瘤微环境,恢复T细胞的抗肿瘤活性,增强机体免疫系统抗肿瘤作用【1】。目前多项临床研究【2-4】已验证,阻断PD1/PD-L1通路具有良好的抗肿瘤效果。
2.产品概述
爱康得生物致力于肿瘤抗体药物的研发,我司自主构建了PD-1 / PD-L1阻断活性检测报告基因系统,该报告基因法可用于测定不同种类的抗PD-1 /PD-L1 mAb的生物活性。该实验包含两个基因工程细胞系:
• PD-1效应细胞:表达human PD-1和NFAT-RE的Jurkat细胞(Jurkat-NFAT-Luc-PD1)
• aAPCCHO-PDL1细胞:表达human PD-L1和CD3抗体的CHO细胞(CHO-S-Anti-CD3-PDL1)。
当Jurkat效应细胞和aAPCCHO-PDL1共培养时,PD-1 / PD-L1相互作用会抑制TCR信号传导和NFAT-RE介导的发光。添加具有阻断活性的PD-1或PD-L1抗体会释放抑制信号,导致TCR激活和NFAT-RE介导的发光(如下图),可以使用Bio-Glo™试剂进行检测和定量。
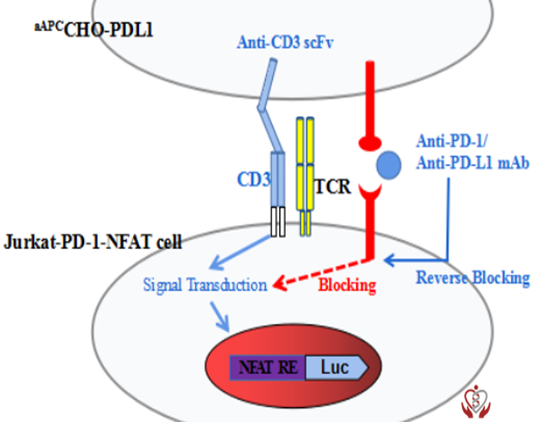
图示说明:当两种细胞共同孵育时, CHO细胞表面抗CD3ScFv 和Jurkat 细胞的膜CD3 分子结合, 向内传递活化信号, 而CHO 细胞表面PD-L1 和Jurkat 细胞表面的PD-1 分子结合, 抑制活化信号的传递, 荧光素酶报告基因不能表达。用这两种细胞模拟了T细胞激活受到PD-1 信号通路抑制的机制, 当加入抗PD-1/PD-L1 抗体时, 阻断PD-1 和PD-L1 的结合, 使CHO 细胞表面抗CD3ScFv和Jurkat 细胞的膜CD3分子结合传递活化信号, NFAT 驱动的荧光素酶报告基因得以表达。
3. 案例展示:
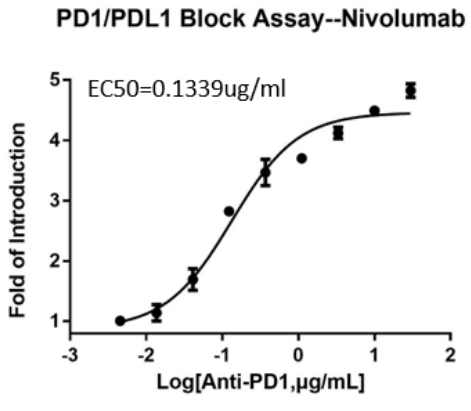
图式说明:基于爱康得构建的Jurkat-NFAT-Luc-PD1/CHO-S-Anti-CD3-PDL1基因报告系统,梯度稀释Nivolumab(起始浓度200nM,5倍梯度稀释9个点),检测抗体阻断活性
4.参考文献:
1.Ma W, Gilligan BM, Yuan J, et al. Current status and perspectives in translational biomarker research for PD-1/PD-L1 immune checkpoint blockade therapy. J Hematol Oncol. 2016;9(1):47. DOI: 10.1186/s13045-016-0277-y
2.Fehrenbacher L, Spira A, Ballinger M, et al. Atezolizumab versus docetaxel for patients with previously treated non-small-cell lung cancer (POPLAR): a multicentre, open-label, phase 2 randomised controlled trial. Lancet. 2016;387(10030):1837-1846. DOI: 10.1016/S0140-6736(16)00587-0
3.Motzer RJ, Escudier B, McDermott DF, et al. Nivolumab versus Everolimus in Advanced Renal-Cell Carcinoma. N Engl J Med. 2015;373(19):1803-1813. DOI: 10.1056/NEJMoa1510665
4.Herbst RS, Baas P, Kim DW, et al. Pembrolizumab versus docetaxel for previously treated, PD-L1-positive, advanced non-small-cell lung cancer (KEYNOTE-010): a randomised controlled trial. Lancet. 2016;387(10027):1540-1550. DOI: 10.1016/S0140-6736(15)01281-7
- 下一篇: ADCC报告基因细胞株

