Nature重要发现:激活MLLT3,血液干细胞体外繁殖能力显著提升!
美国加州大学洛杉矶分校(UCLA)的研究人员近日发现了一种蛋白质与人类血液干细胞自我更新能力之间的联系,激活这种蛋白可导致造血干细胞在实验室条件下自我更新至少12倍。相关研究于11月27日发表在Nature杂志。

DOI:https://doi.org/10.1038/s41586-019-1790-2
血液干细胞(也称为造血干细胞)存在于骨髓中,在那里它们自我更新并分化为各种类型的血细胞。几十年来,骨髓移植一直被用于治疗血液或免疫系统的某些疾病。但是,骨髓移植具有明显的局限性:找到一个相容的骨髓供体并不总是存在的,患者的免疫系统可能排斥异源细胞,并且移植的干细胞数量可能不足以成功治疗疾病。
这就使得在体外条件下增殖血液干细胞成为改善血癌(如白血病)和许多遗传性血液疾病的治疗选择。
UCLA Hanna Mikkola博士团队长期致力于血液干细胞的研究。她说:“尽管多年来我们已经对这些细胞的生物学特性了解很多,但一个关键挑战仍然存在,即人类血液干细胞在实验室中自我更新能力的问题。我们必须克服这一障碍才能推动这一领域向前发展。”
具体来说,将血液干细胞从骨髓中取出并放在实验室培养皿中后,它们很快就会失去自我更新的能力,或死亡,或分化为其他类型的血细胞。Mikkola的目标便是在实验室条件下使血液干细胞自我更新,这将为治疗许多血液疾病开辟新的可能性。
为了找到让血液干细胞在实验室中自我更新的方法,研究人员分析了当人类血液干细胞失去自我更新能力时会关闭的基因,并指出当血液干细胞分化为特定血细胞(如白细胞或红细胞)时哪些基因会关闭。然后他们将血液干细胞放入实验室培养皿中观察。他们还利用多能干细胞,制造出缺乏自我更新能力的血液干细胞样细胞,并监测哪些基因未被激活。
他们发现,MLLT3基因的表达与血液干细胞的自我更新能力密切相关,并且MLLT3基因产生的蛋白质为血液干细胞提供了维持其自我更新能力所需的指令。它通过与其他调节蛋白共同作用来保持血液干细胞的重要部分在细胞分裂时正常运作。
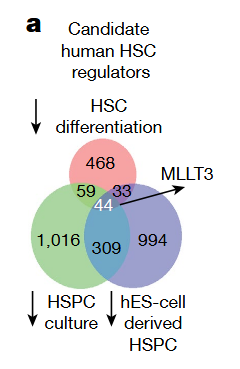
图片来源:Nature
进一步,研究人员想确定,在培养皿中维持血液干细胞中MLLT3蛋白的水平是否足以提高其自我更新能力。为此,该团队使用一种病毒载体(一种经过特殊修饰的病毒,可以将遗传信息携带到细胞核而不引起疾病)将一个活跃的MLLT3基因插入血液干细胞中,并观察到功能性血液干细胞在实验室培养皿中可以繁殖至少12倍。
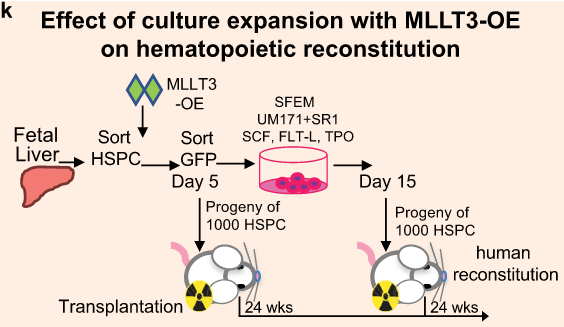
图片来源:Nature
Mikkola说:“治疗一名患者所需的血液干细胞数量极其庞大。但我们不只是关注数量,我们还需要确保实验室制造的血液干细胞在移植时可以通过制造所有类型的血细胞来继续正常工作。”
近期有些研究已经鉴定出一些小分子(通常用于制造药物的有机化合物)有助于人类血液干细胞在实验室中繁殖。当Mikkola的团队使用这些小分子时,他们观察到血液干细胞的自我更新总体上有所改善,但是这些细胞不能维持适当的MLLT3水平,并且在移植到小鼠体内后也不能很好地发挥作用。
“先前关于小分子的发现非常重要,该研究的共同通讯作者Vincenzo Calvanese说,我们以此为基础进行研究,将血液干细胞暴露在这些小分子中,并插入一段活跃的MLLT3基因,从而创造出可以很好融入小鼠骨髓的血液干细胞,有效地产生所有类型的血细胞,并保持它们的自我更新能力。”
值得一提的是,MLLT3使血液干细胞以安全的速率自我更新,且没有任何危险的特征,如增殖过多或突变并产生可能导致白血病的异常细胞。
下一步,研究人员计划确定血液干细胞DNA中的哪些蛋白质和元素会影响MLLT3的开关,以及如何对其进行控制。有了这些信息,他们就有可能找到无需使用病毒载体即可打开和关闭MLLT3的方法,这种方法在临床环境中将更安全。

