最低2.6万元!癌症治愈未来可期
2017年是细胞治疗的元年,美国FDA批准了两项CAR-T疗法。第一款是诺华的Kymriah,第二款是凯特公司(被吉利德收购)研发的Yescarta,两者都用于治疗罹患特定类型的大B细胞淋巴瘤(DLBCL)成人患者,另外Kymriah还用于治疗复发或难治性B细胞急性淋巴细胞白血病(ALL)。
被认为是“清除”癌细胞的绝杀武器的CAR-T疗法自横空出世以来,高昂价格便成为了热门议题。
btw,高昂究竟是多高?
下面,小爱就带大家看一下全球范围内的CAR-T药物定价及医保情况。
两款细胞治疗药在美上市后,Kymriah和Yescarta定价分别为47.5万美元和37.3万美元。
如果加上检查、住院等费用,每名患者花费将达到80万至150万美元。
2018年4月,美国CMS(医疗保险和医疗补助服务中心)宣布,同意为高昂的CAR-T疗法费用买单。具体来说,如果在院外治疗,CMS为接受Kymriah治疗的患者支付约50万美元的费用,为接受Yescarta治疗的患者支付约40万美元的费用,患者仅需支付20%的费用即可。同时,如果是住院治疗,加上副作用维持治疗方面的考虑,最高补助费用可达到150万美元。
此外,CMS还宣布不仅支付CAR-T细胞疗法的费用,还支付所有相关服务费用,包括药物管理、细胞的收集和处理、细胞的回输、以及门诊或者住院的治疗费用,使得CAR-T疗法的费用进一步降低,这无疑是对其他国家CAR-T疗法的费用降低起到了带头作用。
去年8月,欧盟委员会(EMA)同日批准了两款CAR-T疗法KymriahYescarta。
在EMA批准上市后不久,英国国家医疗服务体系(NHS)与诺华Kymriah达成保险覆盖协议,标志欧洲国家首次同意为CAR-T疗法提供资金。
2019年2月,英国国家卫生与临床优化研究所(NICE)发布公告称,复发或难治性DLBCL成年患者可通过CDF获得Kymriah。
2月中旬,苏格兰药品联合会(SMC)批准Kymriah纳入NHS,用于25岁以下患有复发或难治性B-ALL患者,称保密折扣使其“可以接受使用苏格兰NHS的有限资源”。
2018年9月,加拿大卫生部批准了该国首个CAR-T疗法Kymriah,用于治疗3~25岁复发或难治性B-ALL儿科和年轻成人患者,以及复发或难治性大B细胞淋巴瘤的成人患者。
2019年1月,加拿大卫生药品和技术机构(CADTH)称,如果制造商降价,Kymriah应该被公开覆盖,并可能会使加拿大卫生保健系统在三年内花费超过4亿美元。
今年5月,日本将Kymriah的价格定在3300万日元(约合人民币207万元,30.5万美元),医保内批准的适应症为治疗小儿急性淋巴细胞白血病和25岁以下成人弥漫性大B细胞淋巴瘤。
虽然售价昂贵,但Kymriah已被日本纳入医保,这对大部分家庭来说无疑是雪中送炭。就目前日本的医疗保险制度来说,患者自费部分一般占总费用的30%。
除此之外,日本更有“保上保”,即,按照日本公共医疗保险的“高额疗养费制度”来计算的话,使用Kymriah的大部分费用将由日本的公共保险承担,符合条件的患者最低只需负担41万日元(人民币2.57万元)的药费。且只要是持有合法签证,加入日本医保并按期缴纳费用的外国人也适用。
尽管中国目前尚无获批上市的CAR-T疗法,但是根据Insight数据库显示,已有12家企业的CAR-T 疗法获批临床,此外还有25家企业的CAR-T 疗法正在申报临床。
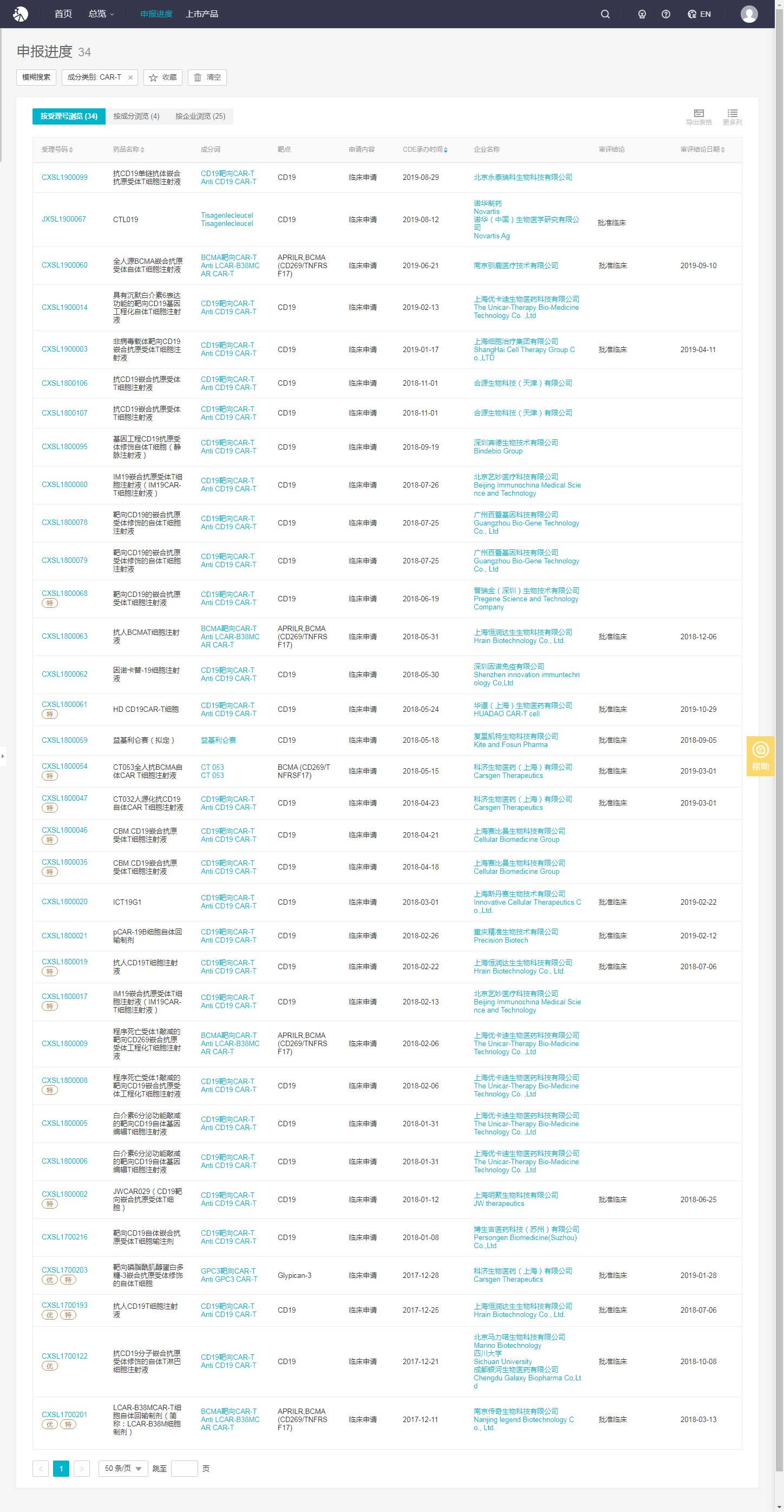
图片来源:https://db.dxy.cn/v5/home
调研数据还显示,截至 2018 年,全球CAR-T细胞治疗市场估值已达一亿六千七百万美元。据 Coherent Market Insights 预测,在 2018-2028 年期间,全球 CAR-T 细胞治疗市场价值将以高达46.1%的平均年复合增长率增长。但随着中国CAR-T相关政策的推进以及研发力度的增强,越来越多的企业涌入CAR-T行业市场,中国有望在未来短时间内弯道超车,占据很大一部分全球市场份额。
随着更多CAR-T疗法进入临床,我们期待,国内CAR-T应用的市场前景将会越来越明朗~
- 上一篇: 一网打尽!2019 CAR-T 研究进展大盘点
- 下一篇: 近期T细胞领域研究进展一览

