生物药研发与生产:高技术壁垒,成本与质量控制核心
生物药研发生产主要包括药物发现、临床前研究、临床试验和商业化生产等阶段。从药物发现开始,到临床研究申请(IND)前,大概需要3-6 年,期间要完成临床前研究,包括工艺开发、技术转移和制造生产三个步骤。IND 审核批准通过后,可以进行临床试验,临床试验一般至少需要进行I、II、III 三期,这个阶段需要6-7 年,在临床试验成功后可向FDA提交生物制品上市许可申请(BLA)。FDA 受理申请文件后,需要进行生物制品上市许可申请批准前检查(PAI),审核通过后,药品可以开始生产上市,这一阶段大概需要0.5-2 年。生物药研发整个流程下来平均需要消耗9.5-15 年的时间,其时间成本、人力物力的投入都是巨大的。
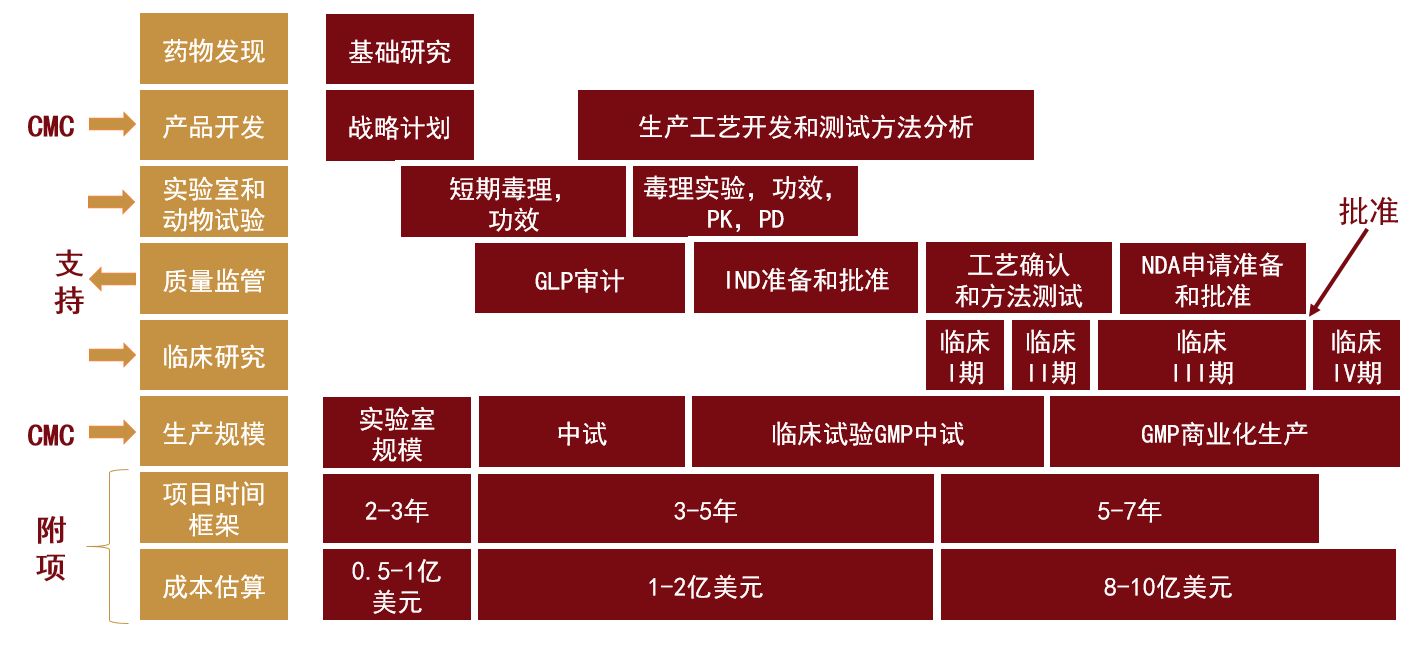
图1:生物药研发时间及商业化成本
1、 壁垒1:发现与制备,转基因小鼠平台Vs 噬菌体展示技术
以目前最为火热的抗体药为例,目前人源抗体的制备主要包括两项技术:转基因小鼠技术和噬菌体展示技术。
转基因小鼠平台:具有高特异性、高亲和力等特点,能大大减少潜在的免疫源性,但是其研发投入大、周期长,也带来一定的局限性。
-
噬菌体展示技术:具有快捷、准确、不受氨基酸位点限制、库容量大等特点,能够模拟天然表位的结构和功能,免疫源性好,生产成本相对低廉,但是该技术仍存在一定的不足之处,容易受到密码子表达偏好性、转化效率、阳性克隆等影响。
1.1人源化转基因小鼠平台
随着单克隆抗体杂交瘤技术的建立,人们在鼠源抗体的基础上逐渐开发出了更具人源亲和性的全人源抗体,转基因小鼠就是生产全人源抗体的一个重要平台。截至2015 年12 月底,FDA 已批准上市12 种通过转基因小鼠平台技术开发的全人源单抗,如安进的evolocumab(antiPCSK9)、nivolumab(anti-PD-1)和denosumab(anti-RANKL)等,以及常用靶点升级抗体药物panitumumab(anti-EGFR)、canakinumab(anti-IL-1β)和ofatumumab
(anti-CD20)等。转基因小鼠在人源抗体药物的研发上具有自身优势,转入小鼠的人免疫球蛋白基因在小鼠的免疫系统中可进行天然抗体的选择机制和成熟机制,使得产生的抗体具备成为药物的天然优势。转基因小鼠平台可通过杂交瘤制备全人源单抗,用于前期的药物研究。目前主要有三大转基因小鼠平台:
Medarex 公司的HuMAb-Mouse:目前已被授权给多家药企使用,从而利用该技术完成了众多靶点的全人源单抗研发。
Abgenix 公司的XenoMouse:2005 年,XenoMouse 技术被Amgen 公司花费22亿美元从Abgenix 公司收购,利用这一平台生产的产品包括Vectibix 等。
Regeneron 公司的Veloclmmune mouse:新一代的转基因小鼠技术平台,该平台不再仅仅可以产生完整的全人源单抗,还可以产生多样化、高质量、特异性强的全人源单抗可变区,这些可变区的编码DNA 可与任何给定的人源恒定区序列进行连接,从而按照预想的方向设计抗体分子,代表产品包括Dupixent 等。
-
另外还有日本协和发酵麒麟的TC Mouse 和KM Mouse,以及Open MonoclonalTechnology(OMT)的OmniMouse
1.2 噬菌体展示技术
噬菌体展示技术是制备人源抗体、小分子抗体和其它各类抗体的另一重要平台,这一技术是应用最广泛的体外抗体筛选技术。产品包括英国Cambridge Antibody Technology 公司(现属于AstraZeneca 公司)的Adalimumab 等。Adalimumab 后被艾伯维公司的购得,商品名为Humira (修美乐),2016 年其销售额高达161 亿美元。
该技术的基本原理是采用生物学手段,在噬菌体基因组中插入抗体基因片段,使噬菌体外壳蛋白表面能够融合表达抗体片段,实现了抗体基因型和表现型的统一,即可用于筛选,也可再次感染宿主菌进行扩增。其中每个噬菌体展示一种抗体,这些重组噬菌体的集合称作噬菌体抗体库,可以方便的用来抗体高通量筛选。从人B 淋巴细胞中扩增抗体基因,可用来构建人源噬菌体抗体库用于抗体筛选。国内代表公司如爱康得生物在该领域积累了丰富的经验。
噬菌体展示技术能够克服免疫耐受,在制备靶向肿瘤、自身抗原、毒性抗原、高度保守的抗原等抗体中具有很大的优势,同时也可采用细胞、组织作为抗原甚至在生物体内筛选抗体,应用广泛,并且筛选效率高。
2、 壁垒2:生物药的表达基础——细胞株的构建
目前,体外重组蛋白的生产主要包括两大系统:原核细胞蛋白表达和真核细胞蛋白表达。不同的表达系统所生产的蛋白在活性和应用方法方面均有所不同。
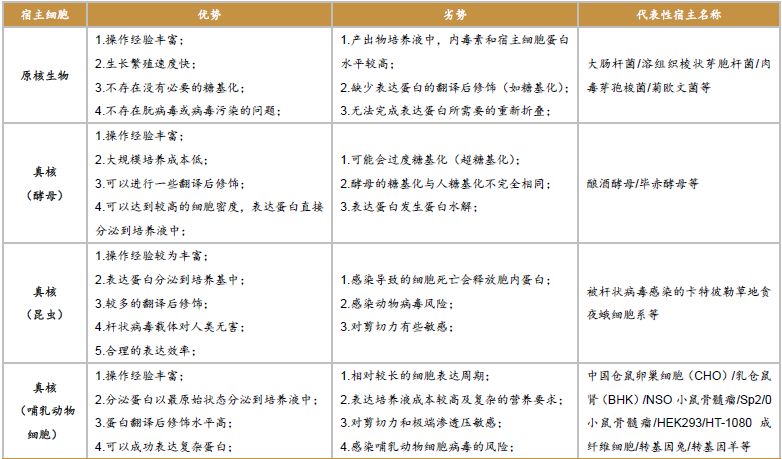
不同表达系统的优缺点对比
2.1 原核细胞表达系统
原核表达系统主要包括大肠杆菌表达系统、乳酸球菌表达系统、芽孢杆菌表达系统这三类。但是原核表达系统的最大问题在于外源蛋白转录后缺乏糖基化和磷酸化修饰,并且原核表达的蛋白无法形成复杂二硫键。当然原核表达也有很多优点:
大肠杆菌:属于革兰氏阴性菌,遗传背景清晰,繁殖速度快,成本低且表达量高。多用于目标蛋白分子量小于100kD,且翻译后修饰作用不影响特定结构和生物活性的蛋白表达。大肠杆菌是目前最常用的原核表达系统,市场上销售的大约30%的重组蛋白产品由大肠杆菌生产,例如部分胰岛素和人生长激素。全球胰岛素市场在2014 年的规模就已经达到了140 亿美元,预计我国2020 年的胰岛素市场可达到760 亿元。代表产品如法国礼来公司(Eli Lilly and Company)的优泌林(Humulin),2017 年上半年销售额6.72 亿美元。
乳酸菌:属于革兰氏阳性菌,膜单一,主要用于大量膜蛋白的表达。
芽孢杆菌:属于革兰氏阳性菌,它能表达并分泌外源蛋白到培养基中,适合分泌型蛋白的生产,如细胞因子或需要形成复杂二硫键的外源蛋白。利用芽孢杆菌表达的外源蛋白包括白细胞介素、人表皮生长因子(hEGF)、胰岛素原等。
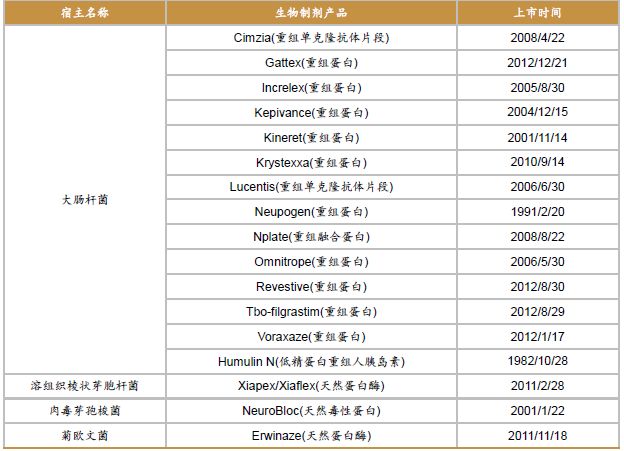
原核表达系统及其代表产品
2.2 真核细胞表达系统
真核细胞表达系统主要包括酵母表达系统、昆虫细胞表达系统、哺乳动物细胞表达系统这三类,此节重点介绍前两类,哺乳动物细胞表达系统在下面的章节详细介绍。
酵母表达系统:酵母中表达的外源蛋白可以进行翻译后修饰,如磷酸化和糖基化。用于外源蛋白表达的酵母菌株包括酿酒酵母、粟酒裂殖酵母、毕赤酵母和乳酸克鲁维酵母。酿酒酵母生产的重组蛋白包括人胰岛素、胰高血糖素、水蛭素类似物、尿酸氧化酶、血小板衍生生长因子等。代表产品如诺和诺德公司生产的诺和灵(胰岛素)系列产品。
昆虫细胞表达系统:可以实现膜蛋白和蛋白激酶的表达。在大多数昆虫细胞表达系统中,外源基因通过杆状病毒载体转染宿主细胞,从而将目标基因通过同源重组插入到宿主的基因组中。昆虫细胞来源的获批药物包括:葛兰素史克的宫颈癌疫苗Cervarix、Valeant 的前列腺癌治疗疫苗Provenge 和Protein Science 的流感疫苗Flublok 等。
2.3 哺乳动物细胞表达系统
目前,哺乳动物细胞表达已成为生物药生产特别是抗体药生产最重要的技术。与酵母等其它真核细胞系相比,哺乳动物细胞表达外源蛋白的优势在于可表达含有复杂二硫键或翻译后修饰的靶蛋白,且蛋白可分泌到培养液中,其产物蛋白的糖基化程度高且均一,有效提高药效,同时减少药物副作用。
中国仓鼠卵巢细胞(CHO)细胞是目前重组蛋白生产领域最具代表性的工程细胞,其具有高效扩增和表达的特点,在补料培养中可达到1-10g/L。据统计,使用CHO细胞系作为表达载体开发的抗体药物超过60%。CHO 细胞从1957 年被首次分离,目前已驯化出多种商业化细胞系,包括CHO-K1、CHO-S 等。
CHO-K1SV 细胞:为龙沙训化的第一代的CHO-K1 细胞系,应用最广泛,已有29种该系统生产的药物获批上市,如罗氏的Zenapax、Medlmmune 的Synagis 等;
CHO-S 细胞是通过驯化筛选生长速度快的CHO 细胞得到的,商品化细胞系以赛默飞世尔的CHO-S 为代表。
目前,越来越多的工程改造细胞系被用于提高药物的质量和产率,如使用ZFNs、TALEN、CRISPR 等基因组编辑技术对CHO 细胞系的基因进行改造。
其它主要哺乳动物细胞系包括HEK293(人胚肾细胞)、HT-1080(人纤维肉瘤细胞)、BHK(乳仓鼠肾细胞)细胞系。
HT-1080 细胞: Agalsidase alfa, Epoetin delta (DYNEPO), Idursulfase
(ELAPRASE) 和Velaglucerase alfa (VPRIV)等。
HEK293 细胞:百健开发的长效八因子Eloctate、长效九因子Alprolix 以及Octapharma 开发的八因子产品Nuwiq 和礼来的GLP-1 产品Trulicity(度拉鲁肽)。
BHK 细胞:常用来表达疫苗产品,用此细胞系表达的上市糖蛋白药物还包括诺和诺德的七因子NovoSeven、拜耳的八因子Kogenate 和百特的猪八因子Obizur。
3、 壁垒3:生物药的生产
生物制品生产工艺的开发过程一般需要经历工程细胞库的构建、摇瓶工艺开发、小试工艺开发、中试放大、生产纯化和制剂等步骤。细胞库通常是三级管理,即原始细胞库(PCB)、主细胞库(MCB)和工作细胞库,其中MCB 和WCB 需要检定合格后并分别于GMP 环境下存放。
另外,根据生物制剂的属性特点不同,会采用不同的哺乳动物细胞进行生产,其中BHK21、CHO 细胞等传代细胞系已证明具有致瘤性,可不必做致瘤性检测;而Vero 细胞因其在一定代次内无致瘤性,则必须做致瘤性检测。
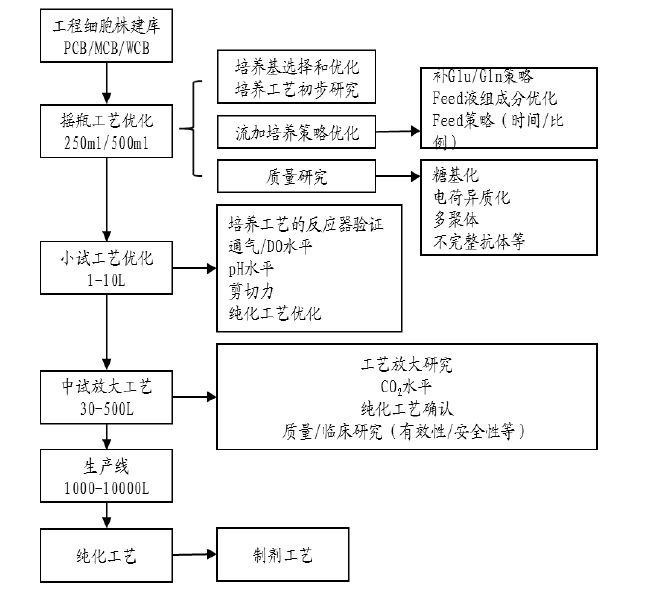
生物制品生产工艺开发流程示意图
- 上一篇: 从抗体到抗体药
- 下一篇: 单克隆抗体作用机制及检测方法要点

