史上最全的免疫检查点阻断抗体副作用的处置
免疫系统在癌症的控制与消除中起着重要的作用。近期通过阻断T细胞上叫做检查点的负调控部分的策略来增强T细胞功能,在患有不同肿瘤的病人身上取得显着效果。CTLA-4抗体易普利姆玛(ipilimumab)被美国FDA批准治疗恶性黑色素瘤,患者的总生存期获益。第二个免疫检查点PD-1与其配体之一PD-L1,作为治疗靶点也显出了很好的应答,Nivolumab和Pembrolizumab(PD-1阻断抗体)已被FDA批准用于治疗晚期黑色素瘤。Nivolumab和Pembrolizumab,或其他PD-1靶向作用抗体,也都对其他肿瘤如非小细胞肺癌,肾细胞癌,膀胱癌以及霍奇金淋巴瘤有效。
虽说这些抗体可以通过增加免疫系统的功能产生确切的治疗效果,然而免疫检查点阻断导致的炎症副作用称为免疫相关性不良反应(irAEs)。免疫相关性不良反应可能会影响任何器官系统,但通常他们会影响皮肤,胃肠道,肝脏和内分泌系统。临时使用免疫抑制药物减弱这些副作用,可能不会减弱抗肿瘤效应。
本文专注于免疫检查点CTLA-4、PD-1和PD-1配体PD-L1阻断抗体引起的免疫相关性不良反应,在黑色素瘤患者中这些药物被广泛研究,经验和建议主要依据黑色素瘤的研究数据。然而随着这些抗体的应用量增长,免疫相关性不良反应的诊断与处置原则在肿瘤学范畴中显得日益重要。
常见的免疫相关性不良反应的类型与处理
皮疹和粘膜刺激
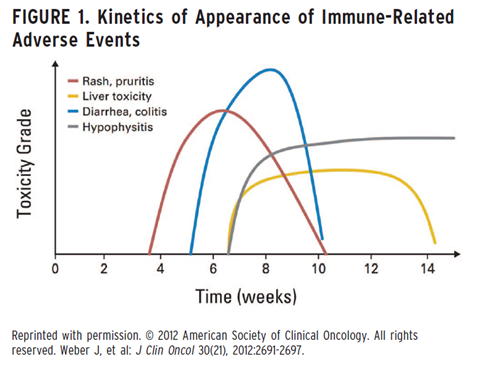
最常见也是最早发生的(图1)与免疫检查点抑制剂相关联的免疫相关性不良反应是皮肤毒性。近50%易普利姆玛(ipilimumab)使用者会发生皮疹并发(或)皮肤瘙痒,与检查点抑制剂相关的皮疹常表现为网状模糊不清的红斑和斑丘疹,通常发生于躯干与四肢。有一例中性粒细胞侵润被诊断为Sweet's Syndrome的报道。也会引起有皮肤白斑/白癜风,通常在检查点抑制剂使用数月后出现。
外用糖皮质激素乳膏可以治疗检查点抑制剂引起的皮疹,口服止痒药物((hy-droxyzine HCl或盐酸苯海拉明)可以治疗检查点抑制剂引起的皮肤瘙痒,严重皮疹(3级以上)需口服糖皮质激素来处理。很少有因检查点抑制剂引起的如Stevens-Johnson综合征/毒性导致皮肤坏死而考虑永久停药的报道。这种情况需要住院并用糖皮质激素静脉给药,并监测体液与电解质
PD-1和PD-L1阻断抗体也可以引起皮肤/粘膜毒性,已有经PD-1/PD-L1治疗的患者出现口腔黏膜炎和口干症状的描述,Nivolumab大规模的一期临床试验中,6.5%患者出现口干的症状,1例患者出现了3度口干症状,口服糖皮质激素或含漱利多卡因可有效治疗这种症状。一些患者反馈有口腔念珠菌感染时有可能在使用免疫抑制剂治疗其他的免疫相关性不良反应,故还需要作出鉴别诊断。
腹泻与结肠炎
腹泻是接受检查点抑制剂治疗后出现的常见症状。而使用CTLA-4靶点抑制剂腹泻发生率比使用PD-1/PD-L1靶点抑制剂腹泻发生率要高得多,在研究这个免疫相关性不良反应时,区别腹泻(排便频率增加)和结肠炎(腹痛,影像学或内窥镜诊断为结肠炎)很重要。使用易普利姆玛(ipilimumab)进行CTLA-4阻断的黑色素瘤患者中,约30%会发生不同程度的腹泻,不到10%患者发生严重(3/4级)腹泻。约5%的接受治疗的患者受到3/4级结肠炎的影响。应告知患者腹泻与结肠炎并不发生在检查点抑制剂治疗初期,而一般发生在大约治疗后的6周(图1)。
使用CTLA-4靶点抑制剂治疗引起腹泻与结肠炎的发生率比使用PD-1/PD-L1靶点抑制剂的高,使用PD-1/PD-L1制剂引起3/4级腹泻概率很低(1%~2%)确切的安全性仍在评估,曾有过明显腹泻与结肠炎患者,接受PD-1治疗后又使用CTLA-4检查点抑制剂治疗期间,也没有引起腹泻与结肠炎的复发。尽管如此,正在进行的临床试验及已掌握的临床经验对全面了解PD-1/PD-L1靶点抑制的安全性是必要的。
当患者出现轻度腹泻,临床医生有必要鉴别是否由其他疾病引起的。如难辨性梭状孢芽杆菌感染或其他细菌/病毒病原体感染。应告知患者多喝水的重要性,一些医生发现美国饮食协会的结肠炎饮食和抗动力药(口服盐酸地芬诺酯和硫酸阿托品,每日4次)会有所帮助。若症状持续超过3天,或症状加重,或/和没有识别到感染病因,那需要口服或静脉给予糖皮质激素。
病情或情况严重,口服糖皮质激素不见好转时,必须住院静脉给予皮质类固醇并进行补水和保持电解质平衡,除非诊断不明,结肠镜检查不是必要的。若静脉给予糖皮质激素(甲基强地松龙2次/天,上限2mg/kg)不能缓解,Infliximab (类克;Janssen生物技术,霍舍姆,宾夕法尼亚)以5mg/kg的剂量每2周给药1次可有所帮助,用Infliximab处置基于患者患有炎性肠道疾病。在极罕见的情况下,结肠炎可导致结肠穿孔,需进行结肠造瘘术。
很遗憾,还没有成熟的方法可防止腹泻的发生。一项研究中使用布地奈德预处理也没有被发现有效,但是一些临床医生发现布地奈德对经饮食调整和使用肠动力拮抗剂后仍持续轻度非感染性腹泻的患者有效。
肝脏毒性
在接受检查点抑制剂患者中肝炎发生,常由谷丙转氨酶(ALT)和谷草转氨酶(AST)升高来判断,总胆红素的升高很少见。但多数患者无症状仅实验室检查异常,部分患者会引起发热。在CTLA-4抑制剂临床试验中ALT和AST升高的发生率在变化,但通常报告的发生率不足10%。PD-1靶点抑制剂大规模临床试验中肝炎发生率同样较低(不足5%),3/4级严重肝毒性更为罕见。
接受治疗的患者中,肝炎的发生大部分在治疗开始的8~12周后,当然也会有提早或延迟出现的情况(图1)影像学检查表现不典型,但在严重的情况下,CT扫描显示轻度肝肿大,门静脉周围水肿或门静脉周围淋巴结肿大。肝活检提示包括肝窦内外浸润重症小叶性肝炎或原发性胆汁样胆小管口周边单核细胞浸润的病理改变。
肝功能(转氨酶和胆红素)应在每次使用易普利姆玛(ipilimumab)前进行监测,如果AST和ALT升高,则需排除病毒和其他药物引起的肝炎的因素。就像治疗其他免疫相关性不良反应一样,如果没有其他明显因素所引起,那么使用糖皮质激素干预是必要的。少数情况下,激素难治性ALT和AST升高可以每12h使用500mg麦考酚吗乙酯(骁悉;Genentech公司,南旧金山,加利福尼亚州)可能会有效,抗胸腺细胞球蛋白治疗也被一个案例报告提及。针对不同的腹泻/结肠炎患者,infliximab不应使用有肝炎的病人,因为infliximab有肝脏毒性的风险。肝炎有可能会持续相当长的时间,并且需要长期或反复递减使用糖皮质激素,也可单独或叠加使用免疫抑制剂。
内分泌失调
免疫相关性不良反应影响到垂体,肾上腺和甲状腺,常会出现非特异性症状如恶心,头痛和疲劳。各临床试验评估、诊断和监控方式的差异,使得内分泌不良反应发生率很难被精确计算。尽管如此,垂体炎(脑垂体炎症)和甲状腺功能减退是最常见的内分泌不良反应,通常认为在接受CTLA-4阻断的病人中发生此不良反应人数达10%。
当被疑似有垂体炎,全部或部分由垂体分泌的激素(促肾上腺皮质激素[ACTH],促甲状腺激素[TSH],卵泡刺激素,促黄体激素,生长激素,催乳素等)会降低。通常垂体炎通过疲劳和头痛等临床症状,影像学检查(垂体增大或肿大),垂体功能低下(ACTH和TSH低下)的生化指标来诊断,垂体相关性生化指标均不同于肾上腺功能低下(低皮质醇或皮质醇激发试验异常,高ACTH)和原发性甲状腺功能减退(低游离T4,高TSH)
当疑似有垂体炎,据说有些临床医生在急性期使用大剂量糖皮质激素(每天1mg/kg强的松)疗程来逆转炎症而不进行必要的长期激素补充。然而就大多数患者而言,因为继发性的甲减(左旋甲状腺激素治疗)或继发性肾上腺功能减退(替代剂量的氢化可的松治疗,一般每天晚上20mg每天早晨10mg)长期激素补充是必要的。也有作者表示患者可以随时成功戒断糖皮质激素补充治疗,但这有可能是个例。垂体炎免疫学机制尚不明确,可能与体液(抗体)免疫的形成损伤垂体或后续的补体激活有关。
在每次使用易普利姆玛(ipilimumab)前都要进行常规甲状腺功能检测(TSH),患者常被诊断出检查点阻断引起的甲状腺功能异常(甲亢或甲减)。普遍认为甲减的发生远多于甲亢,当患者被认为疲劳的症状是内分泌失调引起的时候,把甲减(低游离T4,高TSH)与垂体炎区分开很重要,垂体炎可能会继发甲减(低游离T4低TSH)。甲减的处理涉及甲状腺激素的补充(左旋甲状腺激素)。
最紧急的内分泌失调是与肾上腺危象相关的脱水,低血压及电解质紊乱如高钾血症与低钠血症。如果出现这样的情况,必须住院并且静脉给予糖皮质激素治疗,要与内分泌专家会诊,积极水化和败血症评估至关重要。
接受PD-1/PD-L1阻断治疗的患者出现内分泌失调的几率尚不明确,有可能不同于已发现的CTLA-4阻断引起到的不良反应,很少有公开报道晚期黑色素瘤患者使用PD-1抑制剂引起垂体炎,接受治疗的患者引起甲状腺疾病不足10%。一些病例不良反应可能会加重。PD-1/PD-L1抑制剂引起的内分泌疾病的治疗与CTLA-4阻断引起的相似。
不常受累及器官
肺部
患者接受易普利姆玛(ipilimumab)治疗引起的肺部炎症已被发现,包括结节病和组织炎症性肺炎。使用PD-1抑制剂引起的肺炎在早期试验中有所陈述(10%),并偶有致命的后果。任何患者出现肺部症状,如上呼吸道感染,新发咳嗽或气短,应考虑为肺炎并依据影像学评估。中度或严重的情况下,应在使用免疫抑制剂前利用纤维支气管镜检查以排除感染因素。在严重情况下,应高剂量使用糖皮质激素,如静脉给予2mg/kg的强的松龙。附加其他类型的免疫抑制剂如infliximab,吗替麦考酚酯,环磷酰胺都是可行的。
眼
已有描述使用CTLA-4阻断引起的眼部炎症,包括表层巩膜炎,结膜炎以及葡萄膜炎。该发生率被认为低于1%,症状为畏光,疼痛,眼睛干涩和视力模糊。征求眼科医生的意见,并使用糖皮质激素如1%醋酸泼尼松龙混悬液局部治疗可能受益。严重情况下(3/4级或难治性)可口服糖皮质激素。使用PD-1/PD-L1阻断剂治疗引起的眼毒性没有清晰的描述,这可能由于很少发生有关。
肾脏
一些病例报告中描述使用易普利姆玛(ipilimumab)治疗的患者患有肾功能不全被认为与治疗有关。肾脏组织病理学活检描述了几种不同的病理类型,包括肉芽肿型急性间质性肾炎,膜性狼疮性肾炎。这种情况下口服或静脉给予糖皮质激素来治疗能改善肾功能。有报告部分病例接受PD-1抑制剂并同时阻断CTLA-4和PD-1引起肾功能不全,极少数发生间质性肾炎并对糖皮质激素有应答。
胰腺
接受检查点阻断治疗的患者在无症状的情况下不建议对淀粉酶和脂肪酶作常规检测。同样的淀粉酶和脂肪酶升高而没有其他胰腺炎症状无需用糖皮质激素处理。然而,在有接受CTLA-4和PD-1阻断的患者引起免疫相关性胰腺炎的报道后,当出现临床疑似胰腺炎时都会作淀粉酶和脂肪酶检测。接受CTLA-4和PD-1阻断的临床试验淀粉酶和脂肪酶升高的患者中大部分人无症状,这尚无明确的临床意义,因为他们不符合胰腺炎的诊断标准。
神经系统综合症
神经系统综合症与检查点抑制剂易普利姆玛(ipilimumab)有关。这包括可逆性脑病综合征,无菌性神经炎,肠神经病变和脊髓炎。格林-巴利综合征需格外注意,有一起研究术后使用易普利姆玛(ipilimumab)辅助治疗引起死亡的案例。就如处理其他免疫相关性不良反应,使用糖皮质激素可有效缓解,也应考虑征求神经学专家意见,进行血浆置换术和静脉注射免疫球蛋白。
造血系统综合症
在接受易普利姆玛(ipilimumab)治疗的患者中引起红细胞发育不全,粒细胞减少,获得性A型血友病包括血小板减少都已有描述,类似上述免疫相关性不良反应,通常是使用糖皮质激素进行临时免疫抑制,必要时,尤其在无法明确诊断的情况下可进行骨髓穿刺。
联合使用CTLA-4和PD-1检查点抑制剂的免疫相关性不良反应
由于CTLA-4和PD-1阻断的作用机制不同,故需要对患有不同恶性肿瘤的患者同时使用CTLA-4和PD-1/PD-L1抑制剂进行研究。晚期黑色素瘤患者联合使用易普利姆玛(ipilimumab)和Nivolumab的数据已公布。根据公布数据接受此疗法的患者引起3/4级治疗相关性不良事件发生率约为50%,比单独使用CTLA-4或PD-1/PD-L1抑制剂的引起的不良反应率高。在此项试验中许多3/4级免疫相关性不良反应并无症状,仅实验室检查结果异常。这包括高比例的无症状脂肪酶升高(超过10%),但无一人引发胰腺炎。在联合使用易普利姆玛(ipilimumab)和Nivolumab时,也没发现在单独使用易普利姆玛(ipilimumab)或Nivolumab时没发生过的新毒性。
在其他晚期恶性肿瘤患者中联合使用易普利姆玛(ipilimumab)和Nivolumab的安全性仍在调查研究中。另有研究寻求试验类似CTLA-4和PD-1/PD-L1检查点抑制剂组合的不同抗体。(NCT01975831, NCT02089685, NCT01928394).
检查点抑制剂联合靶向治疗
发现抑制致癌基因蛋白使许多恶性肿瘤的疗效得到提高。其中一个重大发现是靶向作用于黑色素瘤患者突变的BRAF和丝裂原活化蛋白(MAP)激酶途径。基于临床证据显示,RAF可以对免疫产生积极的影响,探索靶向作用于突变BRAF基因的药物和检查点阻断抗体联用将获益很大。
靶向药物联合免疫检查点封闭引发的毒性特征刚开始研究。仅有一份前瞻性研究显示,已被叫停的联合使用Vemurafenib和易普利姆玛(ipilimumab)疗法有较大比例导致3级转氨酶升高,这类组合疗法还需进一步探索。当使用易普利姆玛(ipilimumab)不久后使用Vemurafenib,导致皮疹也是这种组合的重要问题。
易普利姆玛(ipilimumab)与RAF抑制剂联用产生的免疫相关性不良反应类型可能取决于不同的特定的RAF抑制剂。在我的一份独立研究中,Dabrafenib与易普利姆玛(ipilimumab)联合使用,初期还没有发现有重大安全问题。易普利姆玛(ipilimumab)联合Dabrafenib和 Trametinib使用或有更多的问题,因为有患者使用此三联治疗方案会导致严重的结肠炎并穿孔。
下一步将靶向药物联用免疫检查点阻断抗体应用于患有不同疾病的患者的研究还将继续,使用剂量和方法是这种组合疗法的安全和疗效的关键。预计靶向药物联合PD-1/PD-L1抗体比联用易普利姆玛(ipilimumab)副作用更小,当然这个课题还在调查研究之中。
易普利姆玛(ipilimumab)联用粒细胞集落刺激因子
粒细胞-巨噬细胞集落刺激因子(GM-CSF)(莫拉司亭;Genzyme公司,里奇菲尔德,新泽西州)目前未显示能预防或治疗免疫相关性不良反应。但是,GM-CSF联合免疫检查点抑制剂使用是有益的,这基于前期临床数据显示肿瘤疫苗分泌GM-CSF能加强CTLA-4的封闭。在二期随机研究中用GM-CSF和易普利姆玛(ipilimumab)联用治疗晚期黑色素瘤进行测试(易普利姆玛(ipilimumab) 10 mg/kg加GM-CSF和单独使用易普利姆玛(ipilimumab)10mg/kg),目前结果表明,联用能延长患者生存期,较单独使用易普利姆玛(ipilimumab)10mg/kg引起的免疫相关性不良反应要少。
副作用几率降低的机制尚不清楚,但GM-CSF以涉及炎性肠病的发病机制。GM-CSF用于接受易普利姆玛(ipilimumab)上市用量(3 mg/kg)治疗的患者是否能达到类似的效果还尚不清楚。在建议患者常规联合使用GM-CSF和易普利姆玛(ipilimumab)前有必要作进一步的研究。
免疫抑制患者的机会性感染
由于偶尔延长免疫抑制来治疗免疫相关性不良反应,患者会有不常见的机会性感染风险。虽然这些感染,如已报告的极少数曲霉菌性肺炎,但确切的感染率现在还未明朗。根据美国国家综合癌症网络指南对癌症相关性感染的预防与治疗(2B类推荐),每天使用复方新诺明,阿托伐醌或潘他米丁与20mg等效强的松至少4周,可预防杰氏肺囊虫肺炎。抗病毒和抗真菌的预防机制尚不清楚。
免疫介导的不良反应与疗效的相关性调查
检查点阻断抗体引起的免疫相关性不良反应与疗效之间的关系存在争议。患者可以通过使用检查点阻断抗体获益而且不会出现免疫相关性不良反应。PD-1/PD-L1阻断与免疫相关性不良反应之间的任何关联都难以被确定,因为显着的免疫相关性不良反应发生率较低。
有潜在的自身免疫性疾病患者免疫检查点抑制的安全性
不明病因的自身免疫系统疾病(如类风湿关节炎、系统性红斑狼疮)的患者使用检查点抑制剂的安全性尚不清楚。CTLA-4和PD-1具有维持免疫稳态的重要功能,理论上阻断这些受体可能会使潜在的自身免疫性疾病加重。临床前模型表明阻断CTLA-4会加剧免疫性疾病。由于在检查点阻断抗体临床试验中不包含患自身免疫性疾病的患者,所以这方面的临床安全性还需进一步研究。据说部分由潜在自身免疫性疾病的患者已安全使用了易普利姆玛(ipilimumab),但报道了1例有多发性硬化症的患者使用易普利姆玛(ipilimumab)后病情恶化。鉴于检查点阻断抗体对患有危及生命的恶性肿瘤患者巨大的潜在益处,临床医生应与自身免疫性疾病患者深入探讨检查点阻断带来的好处与存在的风险。
结论
免疫检查点抑制剂靶向作用CTLA4和PD-1/PD-L1极大改善了晚期恶性肿瘤患者的状况。治疗会引起常见的暂时性免疫相关性不良反应,但免疫相关性不良反应偶尔可能加重和致命。迅速确认这些副反应并启动全身免疫抑制可以改善预后并且不影响免疫检查点抑制的疗效。虽然还没有前瞻性数据存在来指导最佳的免疫抑制治疗方案,建议遵从根据公认的临床经验而制定的指导方案。免疫检查点抑制剂在不同疾病中的应用和新的联合使用方法的临床经验,将完善免疫相关性不良反应的认识和处置,为取得这种有前景的治疗方法的全部治疗潜力提供了机遇。
- 上一篇: CAR慢病毒表达载体
- 下一篇: 重磅!科学家深入解析CRISPR起源的5个谜团

