CAR-T发现之旅
细胞毒性淋巴细胞(Cytotoxic T Lymphocytes,CTL)在机体中扮演着重要的抗肿瘤角色,通过T细胞受体TCR与抗原肽MHC分子复合物的特异性识别结合形成对肿瘤细胞的监视。但肿瘤细胞的HL LA-I分子表达通常是下调的,这就成为肿瘤细胞逃脱机体免疫监视的重要机制之一,正是由于HLA- I分子的限制,机体内自然产生的TCR很难有效活化并发挥抗肿瘤作用。这使得CTL及相关的细胞免疫治疗的抗肿瘤作用受到了很大的限制。
>
一、CAR结构的设计
自公司成立以来,公司已经为全球客户提供的上百例的CAR-
T服务,除常规的二代、三代CAR分子外,我们在双CAR、增强型CAR、及携带安全开关的CAR分子设计上积累了丰富的经验。此外我们可以为CAR表达载体上安装不同的M
Marker,用于CAR分子表达情况的检测。
二、肿瘤抗原的选择
CAR-
T细胞靶点的选择具有一定的规律性:
第一,该抗原应具有较好的特异性。最理想的抗原应为肿瘤特异性抗原(Tumor specific antigen, TSA),即仅在肿瘤细胞上表达的抗原。但大多数情况下,这类抗原极难发现,因此肿瘤相关性抗原(TAA)是目前大多数CAR- T的靶点。肿瘤相关性抗原往往在正常组织中也有表达,但表达量较肿瘤组织中更少,因此在靶点的选择时应剔除那些会在重要组织中表达的抗原,以避免“On tumor off target”发生的可能。
第二,靶蛋白应选择膜蛋白。部分TSA/TAA为分泌型抗原,此类抗原在血清中浓度较高,当CAR-T细胞回输体内后,游离的抗原与CAR-
T细胞竞争性结合,从而抑制了CAR-T细胞对靶细胞的结合,因此也不合适作为CAR-T的靶点。因此只有膜蛋白是CAR-
T靶点的最佳选择。
三、scFv的获取
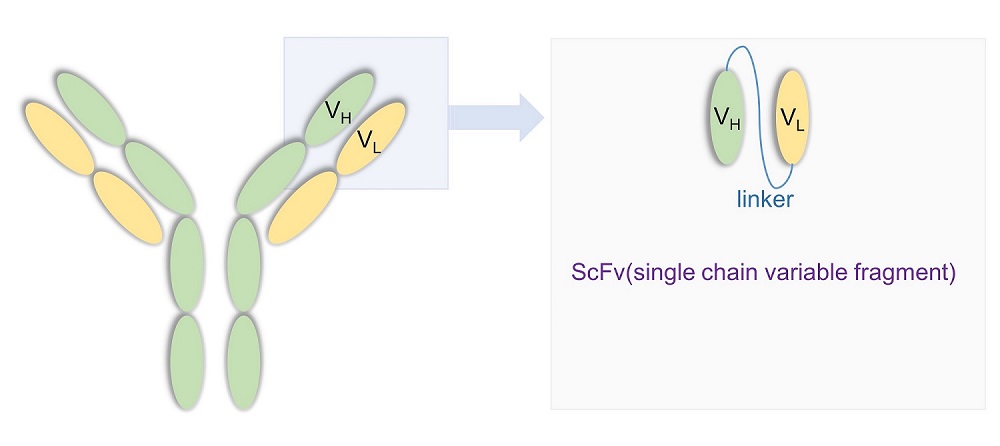
scFv是CAR-T细胞特异性识别肿瘤细胞的关键,其对抗原的亲和力和特异性影响着CAR-
T的有效性和安全性。通过数据库固然可以获得某些抗体的序列,但专利的缺失,限制了未来的产业化。爱康得生物在治疗性抗体筛选领域积累了丰富的经验:在抗原制备环节,我们可
可以提供多种免疫方案,除原核表达系统、酵母表达系统、哺乳动物表达系统获得的重组蛋白以外,我们也可以利用重组细胞株或腺病毒免疫宿主动物,并确保抗体可识别靶蛋白胞外段
段的天然结构;在抗体筛选环节,除传统鼠单克隆抗体筛选服务之外,我们可以进一步提供鼠抗人源化服务,可进一步获得对抗原具有高亲和力和特异性的抗体,此外我们也可以提供纳
纳米抗体和全人源抗体的筛选服务。在此基础上,我们的团队可以为您提供具有自主知识产权的scFv,用于CAR-
T的构建。
四、过表达CAR的慢病毒包装
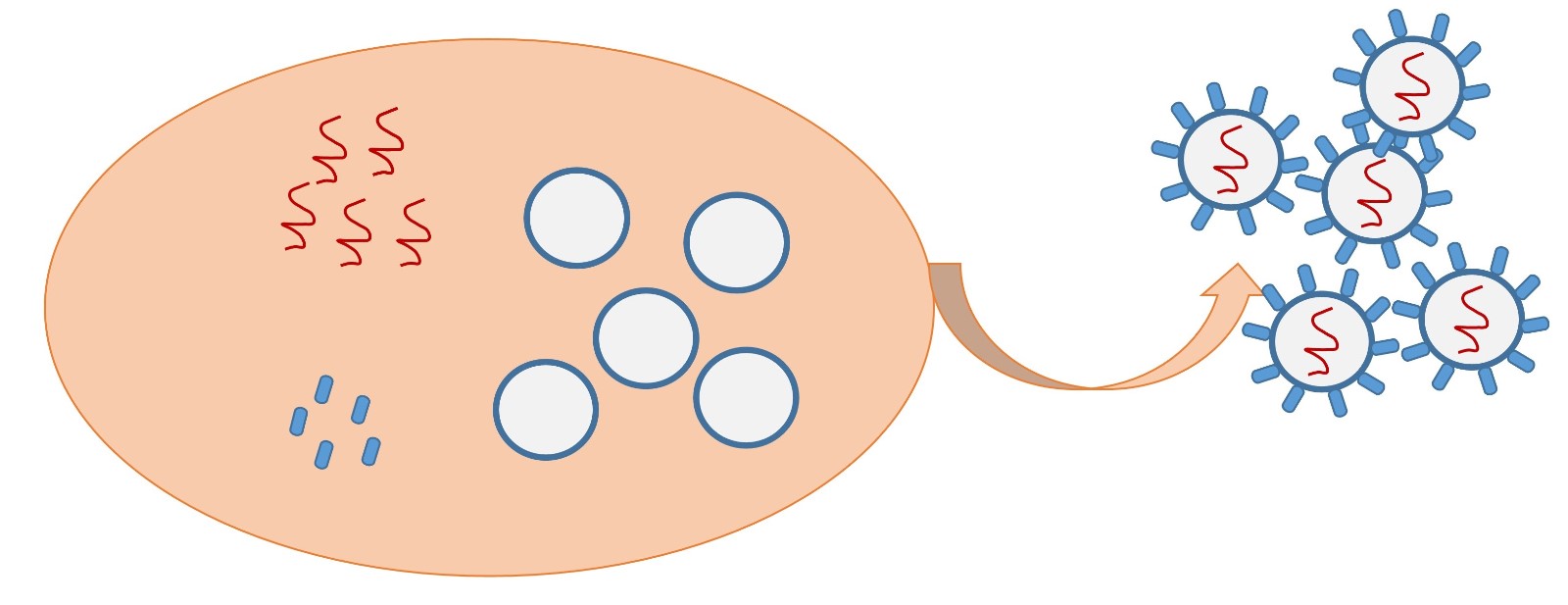
慢病毒是目前最为成熟的基因转染工具之一,利用过表达CAR的慢病毒为载体转染T细胞可获得CAR-
T细胞。除常规的科研级CAR慢病毒以外,为满足基因治疗市场的需求,我们研发了整套无血清临床级慢病毒生产体系,建立了符合GMP要求的整套无血清生产的S.O.P及种子
子细胞库和工作细胞库,公司的慢病毒大规模制备及纯化工艺生产规模可以根据需求从200mL到50L任意设定。我们已经为全球多家临床单位提供临床级慢病毒,满足临床使用需
需求。
五、CAR- T体内外药效学实验
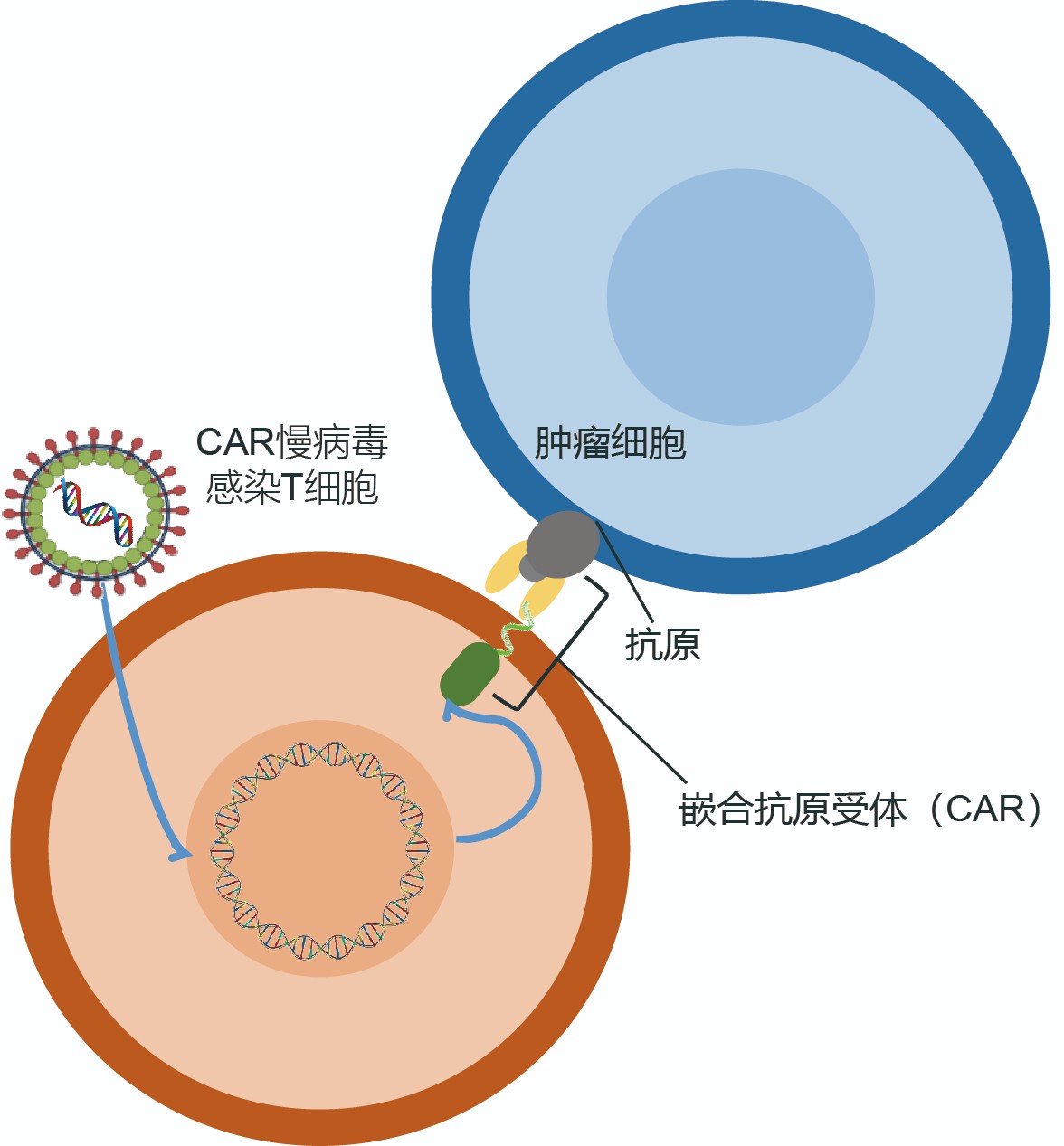
当特异的CAR- T淋巴细胞在体外与靶细胞接触时,可表现出破坏和溶解靶细胞的特性,称为淋巴细胞毒作用(cytotoxicity),即为我们希望的细胞药效。爱康得生物已经为全球近百家 家机构开展了CAR-T细胞的体内外药效学实验。我们可以为您构建所需的过表达细胞株用于细胞/动物模型的构建,通过效靶比实验验证CAR- T细胞的激活程度及对靶细胞的杀伤能力。我们在NGS小鼠成瘤领域也积累了大量的项目经验,构建过数十种小鼠成瘤模型,利用小动物成像系统,可动态检测CAR- T在小鼠体内对肿瘤的杀伤情况。

